Новые публикации
Новые данные способствуют лучшему пониманию причин синдрома Ретта
Последняя редакция: 02.07.2025

Весь контент Web2Health проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.

Синдром Ретта — это редкое нейроразвивающее заболевание, для которого в настоящее время нет ни лечения, ни хорошей терапии. Он вызывает тяжелые физические и когнитивные симптомы, многие из которых перекрываются с расстройствами аутистического спектра.
Синдром Ретта вызывается мутациями в гене MECP2, который сильно экспрессируется в мозге и, по-видимому, играет важную роль в поддержании здоровья нейронов. Ген расположен на X-хромосоме, и синдром в основном поражает девочек. Для разработки терапии синдрома Ретта исследователи хотят лучше понять MECP2 и его функции в мозге.
Исследователи, включая одного из основателей Института Вайтхеда Рудольфа Йэниша, изучают MECP2 на протяжении десятилетий, и, тем не менее, многие базовые факты о гене оставались неизвестными. Белок MECP2, кодируемый геном, участвует в регуляции генов; он связывается с ДНК и влияет на уровень экспрессии различных других генов, то есть на количество белка, которое они производят.
Однако исследователи не имели полного списка генов, на которые влияет MECP2, и не было консенсуса относительно того, как MECP2 влияет на эти гены.
Ранние исследования MECP2 предполагали, что он является репрессором, уменьшающим экспрессию своих целевых генов, но исследования Йэниша и других ранее показали, что MECP2 также действует как активатор, увеличивая экспрессию своих целей — и что он может в первую очередь быть активатором. Также был неизвестен механизм действия MECP2 или что именно делает белок, что приводит к изменениям в экспрессии генов.
Ограничения в технологиях мешали исследователям получить ясность по этим вопросам. Однако Йэниш, постдок в его лаборатории И Лью и бывший сотрудник лаборатории Йэниша Энтони Фламье, ныне доцент исследовательского центра CHU Sainte-Justine в Университете Монреаля, использовали передовые методы для ответа на эти оставшиеся вопросы о MECP2 и получения новых инсайтов о его роли в здоровье мозга и заболеваниях.
Их результаты были опубликованы в журнале Neuron и исследователи также создали онлайн-репозиторий своих данных по MECP2, портал MECP2-NeuroAtlas, в качестве ресурса для других исследователей.
"Я думаю, что эта статья кардинально изменит представления людей о том, как MECP2 вызывает синдром Ретта. У нас совершенно новое понимание механизма, и это может предоставить новые пути для разработки методов лечения этого заболевания," говорит Йэниш, который также является профессором биологии в Массачусетском технологическом институте.
Углубленное понимание MECP2 в мозге
Сначала исследователи создали подробную карту, где в последовательности генов нейронов человека связывается MECP2, либо внутри генов, либо в регуляторных областях ДНК рядом с ними. Они использовали подход, называемый CUT&Tag, который может с высокой точностью выявлять взаимодействия белков с ДНК.
Исследователи обнаружили более четырех тысяч генов, связываемых с MECP2. Они повторили свое картирование в нейронах с распространенными мутациями MECP2, связанными с синдромом Ретта, чтобы определить, где MECP2 исчерпан в состоянии болезни.
Знание того, с какими генами связывается MECP2, позволило Лью и Фламье начать устанавливать связи между целями MECP2 и здоровьем мозга. Они обнаружили, что многие из его целей участвуют в развитии и функционировании аксонов и синапсов нейронов.
Они также сравнили свой список целей MECP2 с базой данных Simons Foundation Autism Research Initiative (SFARI) о генах, связанных с аутизмом, и обнаружили, что 381 ген в этой базе данных является целью MECP2.
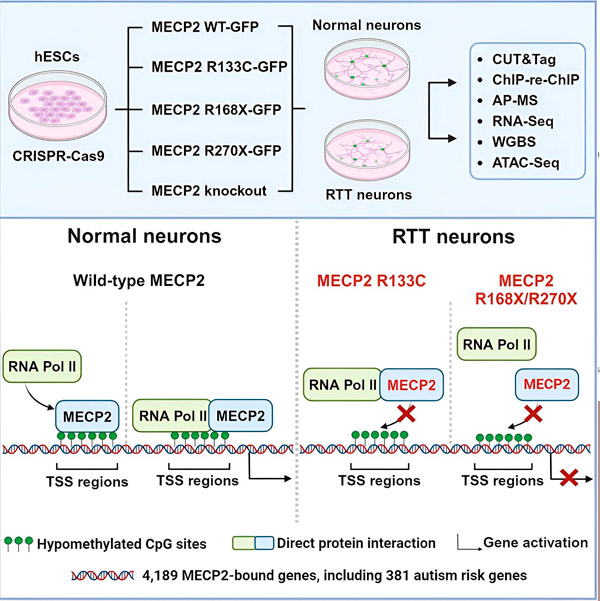
Источник: Neuron (2024). DOI: 10.1016/j.neuron.2024.04.007
Эти находки могут помочь уточнить механизмы, лежащие в основе симптомов аутизма при синдроме Ретта, и предоставляют хорошую отправную точку для исследования возможной роли MECP2 в аутизме.
"Мы создали первую интегрированную карту эпигенома MECP2 в здоровом и больном состоянии, и эта карта может направлять будущие исследования," говорит Лью. "Знание, какие гены являются целями MECP2, и какие гены непосредственно нарушены в болезни, предоставляет прочную основу для понимания синдрома Ретта и задавания вопросов о регуляции генов в нейронах."
Исследователи также изучили, увеличивает или уменьшает MECP2 экспрессию своих целевых генов. В соответствии с историей идентификации MECP2 некоторыми как активатора, а другими как репрессора, Лью и Фламье нашли примеры, где MECP2 играет обе роли.
Однако, хотя MECP2 чаще считается репрессором, Лью и Фламье обнаружили, что он в основном является активатором — подтверждая предыдущие находки Йэниша и Лью. Один новый эксперимент показал, что MECP2 активирует по крайней мере 80% своих целей, а другой — что он активирует до 88% своих целей.
Карта целевых генов, созданная исследователями, предоставила дополнительное понимание роли MECP2 как активатора. Они обнаружили, что для генов, которые активирует MECP2, он обычно связывается с областью ДНК вверх по течению от гена, называемой местом начала транскрипции.
Это место, где клеточные механизмы инициируют процесс считывания гена в РНК, после чего РНК переводится в функциональный белок, который является продуктом экспрессии гена. Присутствие MECP2 в месте начала транскрипции, где начинается экспрессия гена, согласуется с его ролью как активатора гена.
Затем исследователи решили определить, какова роль MECP2 в активации генов. Они изучили, с какими молекулами MECP2 связывается в этом месте, помимо ДНК, и обнаружили, что MECP2 напрямую взаимодействует с белковым комплексом, называемым РНК-полимераза II (RNA Pol II). RNA Pol II является ключевой клеточной машиной, которая транскрибирует ДНК в РНК. RNA Pol II не может самостоятельно находить гены, поэтому ей требуется множество кофакторов или белков-сотрудников, которые помогают ей выполнять свою работу.
Исследователи предполагают, что MECP2 служит одним из таких кофакторов, помогая RNA Pol II инициировать транскрипцию в генах, где связывается MECP2. Структурный анализ MECP2 выявил части молекулы, которые связываются с RNA Pol II, а другие эксперименты подтвердили, что потеря MECP2 снижает присутствие RNA Pol II в соответствующих местах начала транскрипции, а также уровни экспрессии целевых генов.
Это предполагает, что синдром Ретта может быть вызван снижением транскрипции генов, на которые направлен MECP2, из-за мутаций MECP2, которые мешают ему связываться с RNA Pol II или связываться с ДНК. В соответствии с этой идеей, большинство распространенных мутаций MECP2, связанных с болезнью, являются усечениями: мутациями, при которых часть белка отсутствует, что может изменить взаимодействие между MECP2 и RNA Pol II.
Исследователи надеются, что их находки не только изменят наше понимание MECP2, но и что более глубокое и широкое понимание того, как MECP2 влияет на развитие и функционирование мозга, может привести к новым инсайтам, которые помогут людям с синдромом Ретта и связанными расстройствами, включая аутизм.
"Этот проект является отличным примером совместного характера работы лаборатории Йэниша," говорит Фламье. "Рудольф и И имели конкретную проблему, связанную с синдромом Ретта, и у меня был опыт работы с технологией CUT&Tag, которая могла решить эту проблему. Через обсуждение мы поняли, что можем объединить наши усилия, и теперь у нас есть великолепный репозиторий информации о MECP2 и его связях с болезнью."
