Медицинский эксперт статьи
Новые публикации
Экспериментальное моделирование остеоартроза у животных
Последняя редакция: 07.07.2025

Весь контент Web2Health проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
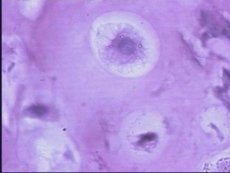
К.Р.Н. Pritzker (1994) определил экспериментальную модель какой-либо болезни у животных как «гомогенную группу животных, у которых имеется унаследованный, естественно приобретенный или экспериментально индуцированный биологический процесс, подвергающийся научному исследованию, который по одному или нескольким параметрам схож с болезнью у человека». Модели остеоартроза у животных удобны для исследования эволюции структурных изменений в суставных тканях для выяснения того, как различные факторы риска их инициируют или способствуют появлению этих изменений, а также для опенки применяемых терапевтических мер. Необходимо помнить, что остеоартроз - это заболевание не одной ткани - суставного хряща, а всех тканей пораженного сустава, включая субхондральную кость, синовиальную оболочку, мениски, связки, периартикулярные мышцы и афферентные нервы, окончания которых лежат как снаружи, так и внутри суставной капсулы. Проводимые исследования фармакологических агентов на моделях у животных фокусируются главным образом на их влиянии на суставной хрящ. На экспериментальных моделях невозможно оценить главный симптом остеоартроза у людей - боль в суставах. В то же время при моделировании остеоартроза у животных не учитывают ряд важных факторов, способствующих развитию и прогрессированию остеоартроза (например, вертикальное положение тела человека, слабость периартикулярных мышц и др.).
Разумеется, наиболее наглядной моделью болезни является та, которая имеет наибольшее сходство с изменениями при остеоартрозе у человека. Наибольший интерес модели остеоартроза у животных представляют в плане исследования эффективности препаратов, «модифицирующих болезнь» (DMOAD - disease modifying OA drugs). Несмотря на то, что ряд препаратов этой группы предотвращают развитие или замедляют прогрессирование экспериментально-индуцированного или спонтанного остеоартроза у животных, при изучении их действия у человека все они оказались неэффективными.
Модели остеоартроз у животных
|
Механизм модели-рования |
Вид животных |
Индуцирующий фактор/агент |
Источник |
|
Спонтанный остеоартроз |
Морские свинки |
Возраст/избыточная масса тела |
Bendele A.M. etal., 1989 |
|
Мыши STR/ORT, STR/INS |
Генетическая предрасположенность |
Das-Gupta E.P. et al., 1993 Dunham J. etal., 1989 Dunham J. etal., 1990 |
|
|
Черные мыши С57 |
Генетическая предрасположенность |
OkabeT., 1989 StabescyR. etal., 1993 TakahamaA.. 1990 van der Kraan P.M. etal., 1990 |
|
|
Мыши |
Мутация коллагена II |
GarofaloS. etal., 1991 |
|
|
Мыши |
Мутация коллагена IX |
NakataK. etal., 1993 |
|
|
Собаки |
Дисплазия тазобедренного сустава |
SmaleG. etal., 1995 |
|
|
Приматы |
Генетическая предрасположенность |
Alexander C.J., 1994 Carlson C.S. etal., 1994 ChateauvertJ.M. etal., 1990 |
|
|
Химически индуци-рованный остеоартроз |
Цыплята |
Иодоацетат в/с* |
Kalbhen DA, 1987 |
|
Кролики |
Папаин в/с |
MarcelonG. etal., 1976 CoulaisY. etal., 1983 CoulaisY. etal., 1984 |
|
|
Морские свинки |
Папаин в/с |
TanakaH. etal., 1992 |
|
|
Собаки |
Химопапаин в/с |
Leipold H.R. etal., 1989 |
|
|
Мыши |
Папаин в/с |
Van der Kraan P.M. etal., 1989 |
|
|
Мыши |
Коллагеназа в/с |
Van der Kraan P.M. etal., 1989 |
|
|
Мыши |
ТФР-Р в/с |
Van den Berg W.B.. 1995 |
|
|
Кролики |
Гипертонический раствор NaCI |
VasilevV. etal.. 1992 |
|
|
Физически (хирургически) индуци-рованный остеоартроз |
Собаки |
Пересечение передней крестообразной связки (унилатерально) |
Marshall J.L etal., 1971 Brandt K.D., 1994 |
|
Собаки |
Пересечение передней крестообразной связки (билатерально) |
Marshall K.W.. Chan A.D., 1996 |
|
|
Кролики |
Пересечение передней крестообразной связки |
Christensen S.B., 1983 VignonE. etal., 1991 |
|
|
Овцы |
Менискэктомия |
Ghosh P. etal., 1993 |
|
|
Кролики |
Менискэктомия |
FamA.G. etal., 1995 Moskowitz R.W., Goldberg V.M., 1987 |
|
|
Морские свинки |
Менискэктомия |
Bendele A.M., 1987 |
|
|
Морские свинки |
Миоэктомия |
ArseverC.L, BoleG.G., 1986 LaytonM.W. etal., 1987 Dedrick D.K. etal., 1991 |
|
|
Кролики |
Контузия коленной чашечки |
OegemaT.R.J, etal., 1993 MazieresB. etal., 1990 |
|
|
Кролики |
Иммобилизация |
Langenskiold A. et al., 1979 Videman Т., 1982 |
|
|
Собаки |
Иммобилизация |
Howell D.S. etal., 1992 Ratcliffe A. et al., 1994 PalmoskiM., Brandt K.D, 1981 |
|
|
Собаки |
Денервация с последующим пересечением передней крестообразной связки |
VilenskyJA etal., 1994 |
* в/с - внутрисуставно.
Физически и химически индуцированные модели остеоартроза очень популярны в настоящее время, однако они скорее отражают процессы, которые наблюдаются при вторичном остеоартрозе у человека, чем при идиопатическом. Альтернативой им являются модели спонтанного остеоартроза у двуногих приматов и четвероногих животных.
Некоторые авторы весьма скептически относятся к моделированию остеоартроза у животных вообще. Так, по мнению M.E.J. Billingham (1998), использование моделей для открытия модифицирующих остеоартроз препаратов представляет собой «...дорогостоящую авантюру».
Модели спонтанного остеоартроза
Практически у всех инбридных линий мышей развивается остеоартроз различной степени тяжести и локализации. Наиболее высокую заболеваемость остеоартрозом и наиболее тяжелое течение болезни наблюдают у мышей линий STR/ORT и STR/INS. Среди мышей линии STR/ORT заболевание более распространено, оно более тяжело протекает у самцов, чем у самок. Первичное повреждение суставного хряща развивается в медиальной части пластинки большеберцовой кости. Предполагалось, что появлению изменений в хряще предшествует смешение надколенника, однако R.G. Evans и соавторы (1994), С. Collins и соавторы (1994) обнаружили, что у всех мышей этой линии повреждение хряща развивается к 11 мес, однако не у всех выявлено смещение надколенника. Эти же авторы обнаружили, что изменениям в суставном хряще у мышей линий STR/ORT часто предшествует хондроцитарно-остеобластная метаплазия клеток сухожилий и связок вокруг пораженных коленных суставов, что указывает на первичность этих изменений в патогенезе остеоартроза в данной модели. Возможно, что первичная кальцификация связок и сухожилий изменяет механическое давление на внутрисуставные структуры и дальнейшие изменения в суставном хряще отражают попытку поддержать нормальную нагрузку на сустав. В отличие от моделей с использованием морских свинок и макак, у которых дегенерации хряща предшествуют изменения в субхондральной кости, у мышей линий STR/ORT и STR/INS субхондральный склероз появляется позже.
Преимуществом данной модели остеоартроза является небольшой размер животных, требующий минимального расхода испытуемого фармакологического агента. Однако размер также является и недостатком, поскольку у мышей затруднен биохимический, патогистологический анализ хряща.
Исследования А.М. Bendele, J.E Hulman (1988), А.М. Bendel и соавторов (1989), а также S.C.R. Meacock и соавторов (1990), посвященные изучению естественного течения спонтанного остеоартроза у морских свинок, активизировали интерес к этой модели болезни. Начиная с возраста 13 мес у всех самцов морских свинок линии Dunkin Hurtley появляется дегенерация суставного хряща. Аналогичные изменения у самок появляются несколько позже и носят более мягкий характер. В возрасте 1 год наблюдают полную потерю суставного хряща в области медиального мыщелка бедренной кости и пластинки большеберцовой кости. Увеличение массы тела морских свиноклинии Dunkin Hurtley усугубляет течение болезни, а уменьшение массы тела до 900 г и меньше улучшает течение остеоартроза. В возрасте 8 нед в этой модели уже обнаруживают изменения субхондральной кости, т.е. последние предшествуют поражению хряща. Изменения крестовидных связок коленных суставов могут ускорять ремоделирование костной ткани.
Спонтанный остеоартроз развивается у макак rhesus и cynomolgus. Очень важным преимуществом приматов перед другими животными, используемыми для создания экспериментальной модели остеоартроза, является двуногость. Заболевание развивается у особей среднего/пожилого возраста. Ранними гистологическими находками являются утолщение субхондральной кости с последующим разволокнением суставного хряща в области медиальной пластинки болылеберцовой кости. В дальнейшем в процесс вовлекается и латеральная пластинка. Примечательно, что дегенерация суставного хряща начинает развиваться только после того, как толщина субхондральной кости достигнет 400 мкм. Рост распространенности и степени тяжести остеоартроза у макак происходит с возрастом, однако на эти показатели не влияют пол и масса тела. До настоящего времени модели остеоартроза у приматов не использовали для изучения эффективности DMOADs.
Модели физически (хирургически) индуцированного остеоартроза
Модели остеоартроза, основанные на хирургически индуцированной разболтанности коленных суставов, изменяющей механическое давление на них, наиболее часто используют у собак и кроликов. Наиболее широко применяют модель с пересечением крестовидных связок у собак. При создании хирургических моделей остеоартроза у кроликов используют операции по пересечению крестовидных связок с иссечением медиальных и коллатеральных связок или без такового, тотальную или парциальную менискэктомию, хирургический разрыв менисков. У морских свинок описаны хирургические модели остеоартроза, созданные путем пересечения крестовидных и коллатеральных связок, частичной менискэктомии. Частичная менискэктомия у морских свинок ведет к образованию остеофитов в течение 2 нед и избыточной дегенерации суставного хряща в течение 6 нед.
До недавнего времени к модели остеоартроза у собак, развившемуся после пересечения передних крестовидных связок, относились скептически в связи с отсутствием ульцерации хряща и заметного прогрессирования болезни, наблюдаемых при остеоартрозе у человека. J. L. Marshall и S. - Е. Olsson (1971) обнаружили, что изменения в тканях коленных суставов у собак через 2 года после операции практически не отличались от зарегистрированных сразу после нее. Авторы предположили, что механические факторы (например, фиброз суставной капсулы и образование остеофитов) стабилизируют разболтанный после операции коленный сустав и препятствуют дальнейшему прогрессированию разрушению суставного хряща. Также было предложено считать данную модель моделью повреждения и репарации хряща, а не моделью остеоартроза. Однако результаты исследований, проведенных K.D. Brandt и соавторами (1991), которые более длительно изучали динамику изменений в тканях коленных суставов, дестабилизированных пересечением передних крестовидных связок, опровергли предположения предыдущих авторов.
С.А. McDevitt и соавторы (1973, 1977) обнаружили, что уже в течение первых дней после пересечения крестовидных связок увеличивается синтез протеогликанов хондроцитами суставного хряща. В течение 64 нед после хирургического индуцирования нестабильности коленного сустава толщина суставного хряща была выше нормы, хотя биохимические, метаболические и гистологические изменения в нем соответствовали таковым при остеоартрозе. Это утолщение хряща ассоциировалось с повышенным синтезом протеогликанов и их высокой концентрацией в суставном хряще. Используя магнитно-резонансную томографию (MPT), M.E. Adams и K.D. Brandt (1991) показали, что после пересечения крестовидных связок гипертрофия хряща поддерживается в течение 36 мес, в дальнейшем возникает прогрессирующая потеря хряща, так что уже через 45 мес большая часть суставных поверхностей лишена хряща. Морфологическое исследование хряща через 54 мес после операции подтвердило результаты МРТ. Таким образом, М.Е. Adams и K.D. Brandt (1991) доказали, что хирургически индуцированную нестабильность коленных суставов у собак можно считать моделью ОА.
Феномен гипертрофической репарации суставного хряща хорошо иллюстрирует вышеописанная модель остеоартроза у собак. Однако известно, что данный феномен присущ не только ей. Гипертрофия суставного хряща, которая носила репаративный характер, впервые была описана у больных с остеоартрозом E.G.L. Bywaters (1937), а впоследствии L.C. Johnson. Ее также обнаруживают и в других моделях остеоартроза - у кроликов после частичной менискэктомии (Vignon E. et al., 1983), у макак rhesus гипертрофия хряща развивается спонтанно.
Современное описание патогенеза акцентируется главным образом на прогрессирующей «потере» хряща, однако часто авторы упускают из виду его утолщение и усиление синтеза протеогликанов, что соответствует гомеостатической фазе стабилизированного остеоартроза. В течение этой фазы репарация хряща компенсирует его потерю и может поддерживать сустав в функциональном состоянии длительное время. Но репаративная ткань часто не может справляться с возложенной на нее механической нагрузкой так, как это делает здоровый суставной хрящ, что приводит к неспособности хондроцитов поддерживать нормальный состав матрикса и снижению синтеза протеогликанов. Развивается конечная стадия остеоартроза.
Изучение артропатии Шарко привело к появлению метода нейрогенного ускорения моделирования хирургически индуцированного остеоартроза. Артропатия Шарко характеризуется тяжелой деструкцией суставов, суставными «мышами», выпотом в сустав, нестабильностью связок, образованием новой костной и хрящевой ткани в пределах сустава. Общая концепция патогенеза артропатии Шарко (нейрогенной) заключается в прерывании чувствительных сигналов от проприорецепторов и ноцицепторов конечностей в центральную нервную систему (ЦНС). Для ускорения прогрессирования остеоартроза, индуцированного пересечением передних крестовидных связок у собак, перед операцией выполняют ганглийэктомию или иссечение иннервирующего сустав нерва, что приводит к появлению эрозий хряща уже в первую неделю после операции. Интересно, что новый DMOAD диацереин оказался эффективным при использовании на медленно прогрессирующей (нейрологически интактной) модели остеоартроза, однако при нейрогенно ускоренном экспериментальном остеоартрозе препарат оказался неэффективным.
В заключение необходимо отметить, что невозможно полностью оценить идентичность экспериментальной модели остеоартроза и остеоартроза у человека, поскольку этиология и точные механизмы патогенеза заболевания к настоящему времени не выяснены. Как указывалось ранее, основной задачей использования экспериментальных моделей остеоартроза у животных является их использование для оценки эффективности новых препаратов, главным образом группы «модифицирующих болезнь». Вероятность того, насколько результаты лечения животного совпадут с результатами применения экспериментального фармакологического агента у человека, также невозможно определить. N.S. Doherty и соавторы (1998) акцентировали внимание на значительных различиях между видами животных, используемых для моделирования остеоартроза, в плане разного развития патологии, различных медиаторов, рецепторов, ферментов, что приводит к необъективной экстраполяции терапевтической активности новых препаратов, используемых у животных, на человека. Примером может быть высокая эффективность НПВП при моделировании воспалительного артрита у грызунов. Это привело к переоценке эффективности НПВП у человека, у которого простагландины не играют той фундаментальной роли в патогенезе заболевания, которую они играют у грызунов, а клиническая эффективность НПВП скорее ограничена лечением симптомов, чем модификацией болезни.
В то же время недооценка новых фармакологических агентов при изучении их эффективности на моделях у животных может привести к утрате потенциально эффективных у человека терапевтических агентов. Например, соли золота, пеницилламин, хлорохин и сульфазалазин, обладающие определенным эффектом при терапии ревматоидного артрита, абсолютно не эффективны у животных, которых используют для скриннинга антиревматических препаратов.
Отличие ответа животного с моделированным остеоартрозом и больного с остеоартрозом на лечение DMOAD во многом зависит от коллагеназы - фермента, который, как полагают, принимает активное участие в патогенезе остеоартроза. У грызунов с моделированным ОА часто обнаруживают ингибиторы интерстициальной коллагеназы (коллагеназы-1 или матричной металлопротеиназы (ММП)-1), однако гомолог коллагеназы-1 человека у грызунов не найден, возможно, его не существует. Таким образом, специфические ингибиторы коллагеназы-1 человека не проявят терапевтическую эффективность у грызунов с экспериментальным остеоартрозом. Большинство ингибиторов ММП, созданных к настоящему времени, неселективные и поэтому угнетают коллагеназу-3 (ММП-13), участвующую в патогенезе экспериментального остеоартроза у грызунов. Более того, как показали исследования N.R.A. Beeley и соавторов (1994), J.M.P. Freije и соавторов (1994), коллагеназа-3 человека экспрессируется в суставном хряще больных с остеоартрозом и, возможно, играет роль в патогенезе заболевания.
Можно предположить, что данные медиаторы, рецепторы или ферменты играют аналогичную роль в патогенезе моделированного остеоартроза у определенного животного и у человека. Примером может служить хемотаксическая способность лейкотриена В4, которая у человека, мыши и кролика считается одинаковой, однако активность антагонистов этого биологически активного вещества между видами животных различается в 1000 раз. Для того чтобы избежать подобных неточностей в экспериментах, необходимо создать методы, позволяющие исследовать фармакодинамику in vivo. Например, можно изучать влияние каких-либо веществ на активность экзогенных ферментов или медиаторов человека. Эта методика была применена V Ganu и соавторами (1994) для оценки активности ингибиторов ММП путем определения способности препаратов угнетать высвобождение протеогликанов из суставного хряща после инъекции стромелезина человека в коленный сустав кролика.
Несмотря на то что результаты, полученные в эксперименте на моделированном остеоартрозе, могут привести к неправильной оценке потенциальных DMOAD, модели остеоартроза у животных играют важную роль в базисных исследованиях. Окончательное же решение об эффективности фармакологических агентов в терапии болезней человека можно сделать только после проведения III фазы клинических испытаний у человека.


 [
[