Новые публикации
Учёные отслеживают самые ранние физические изменения в клетках, вызывающие рак
Последняя редакция: 02.07.2025

Весь контент Web2Health проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Когда рак диагностируется, за этим уже стоит множество событий на клеточном и молекулярном уровнях, которые происходили незаметно. Хотя рак классифицируется на ранние и поздние стадии в клинических целях, даже опухоль на "ранней" стадии является результатом многих предшествующих изменений в организме, которые невозможно было обнаружить.
Теперь ученые из Медицинской школы Йельского университета (YSM) и их коллеги получили детальное представление о некоторых из этих ранних изменений, используя мощную микроскопию высокого разрешения для отслеживания самых первых физических изменений, вызывающих рак, в клетках кожи мышей.
Изучая мышей, несущих мутацию, способствующую развитию рака в их волосяных фолликулах, ученые обнаружили, что первые признаки формирования рака происходят в определенное время и в определенном месте в росте волосяных фолликулов мышей. Более того, они обнаружили, что эти предраковые изменения можно заблокировать с помощью лекарств, известных как ингибиторы MEK.
Команду возглавил Тяньчи Синь, доктор философии, научный сотрудник кафедры генетики YSM, и включала Валентину Греко, доктора философии, профессора генетики YSM и члена Йельского онкологического центра и Йельского центра стволовых клеток, а также Сержи Регота, доктора философии, доцента молекулярной биологии и генетики в Медицинской школе Джонса Хопкинса.
Результаты их исследований были опубликованы в журнале Nature Cell Biology.
Ученые изучили мышей, развивающих кожную плоскоклеточную карциному, второй по распространенности тип рака кожи у людей. Эти мыши были генетически модифицированы с мутацией, способствующей развитию рака, в гене KRAS, который является одним из самых часто мутировавших онкогенов в человеческих раках. Мутации KRAS также были обнаружены при раке легких, поджелудочной железы и колоректальном раке.
Ранние изменения, которые изучили ученые, включали рост крошечного, ненормального бугорка в волосяном фолликуле, что классифицируется как предраковая аномалия. "Понимание этих ранних событий может помочь нам разработать подходы для предотвращения окончательного формирования рака", сказал Синь, первый автор исследования.
Хотя их исследование сосредоточено на раке кожи, исследователи считают, что принципы, которые они обнаружили, могут быть применены к многим другим видам рака, вызванным мутациями KRAS, потому что основные гены и белки, вовлеченные в эти процессы, одинаковы для разных опухолей.
Не просто пролиферация клеток Как у людей, так и у мышей волосяные фолликулы постоянно растут, теряя старые волосы и формируя новые. Стволовые клетки, которые имеют способность развиваться в различные типы клеток, играют большую роль в этом процессе обновления. Предыдущие исследования показали, что мутации KRAS приводят к увеличению пролиферации стволовых клеток в волосяных фолликулах, и считалось, что это значительное увеличение количества стволовых клеток отвечает за предраковое нарушение тканей.
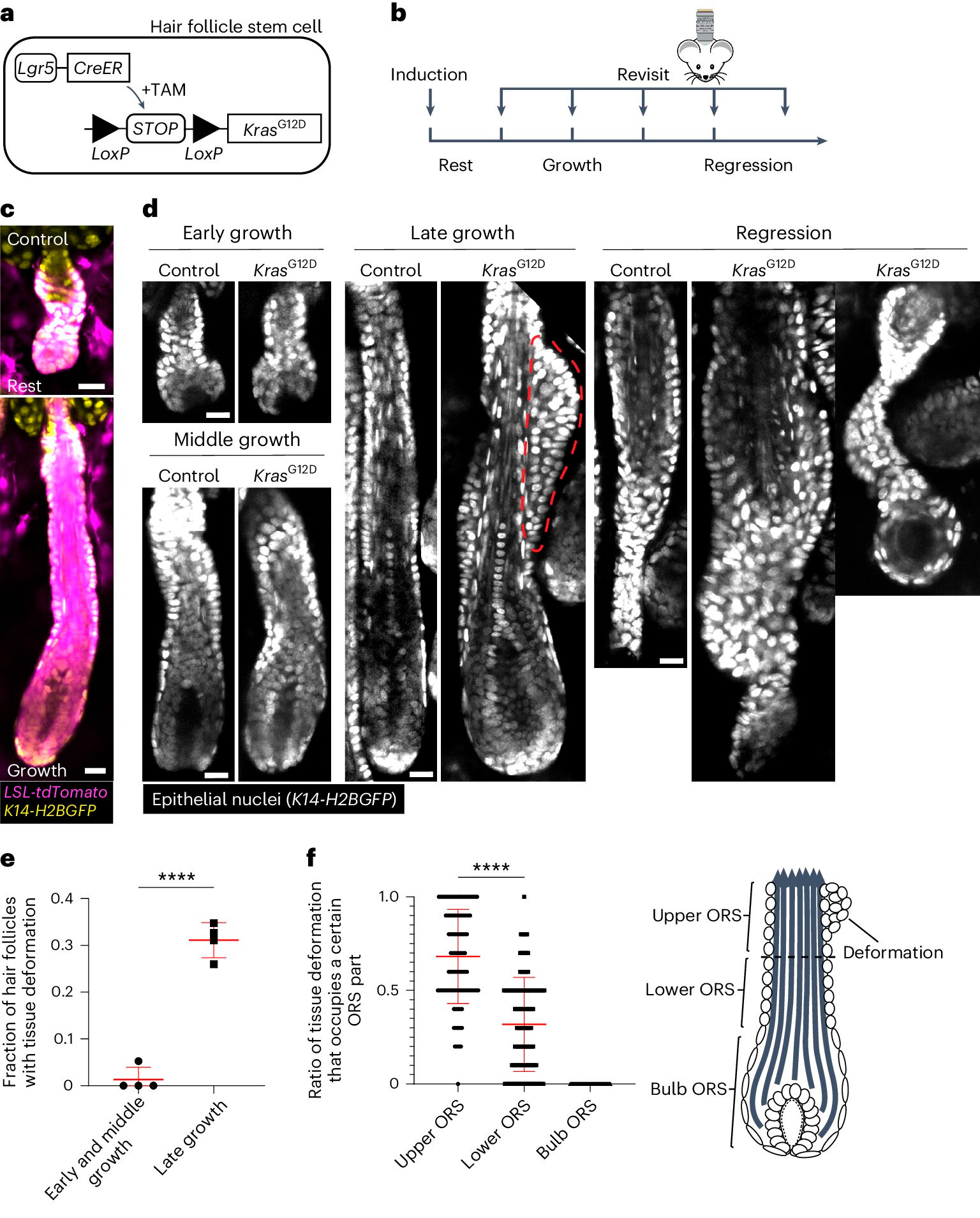
KrasG12D вызывает пространственно-временные специфические деформации тканей при регенерации волосяных фолликулов.
A. Схема генетического подхода для индукции KrasG12D в стволовых клетках волосяного фолликула с использованием системы Cre–LoxP, индуцируемой тамоксифеном (TAM).
B. Схема, показывающая время индукции KrasG12D и повторной визуализации относительно стадий цикла роста волос.
C. Представительные изображения диких типов покоящихся и растущих волосяных фолликулов, содержащих индуцируемый Cre tdTomato (магента) репортер после индукции.
D. Представительные изображения контрольных и KrasG12D волосяных фолликулов на разных стадиях цикла роста волос. Деформация ткани в виде бугорков в наружной корневой оболочке (ORS) обозначена красной пунктирной линией.
E. Доля KrasG12D волосяных фолликулов с деформацией ткани на разных стадиях роста волосяного фолликула.
F. Доля деформаций ткани, занимающих верхнюю, нижнюю и луковичную части ORS для отдельных KrasG12D волосяных фолликулов.
Источник: Nature Cell Biology (2024). DOI: 10.1038/s41556-024-01413-y
Чтобы проверить это предположение, команда использовала специально разработанную форму мутированного KRAS, которую они могли активировать в определенное время в клетках кожи волосяных фолликулов животных. Синь и его коллеги использовали метод микроскопии, известный как интра-витальная визуализация, который позволяет получать изображения клеток с высоким разрешением в живом организме и отмечать и отслеживать отдельные стволовые клетки в животных.
Когда мутация KRAS была активирована, все стволовые клетки начали пролиферировать быстрее, но предраковый бугорок образовался только в одном конкретном месте в волосяном фолликуле и на одной стадии роста, что означало, что общее увеличение числа клеток, вероятно, не было всей историей.
Активация мутации KRAS в волосяных фолликулах привела к более быстрой пролиферации стволовых клеток, изменению их миграционных паттернов и делению в разных направлениях по сравнению с клетками без мутации, способствующей раку.
Мутация воздействует на белок, известный как ERK. Синь смог наблюдать активность ERK в реальном времени в отдельных стволовых клетках в живых животных и обнаружил специфическое изменение в активности этого белка, вызванное мутацией KRAS. Исследователи также смогли остановить образование предракового бугорка с помощью ингибитора MEK, который блокирует активность ERK.
Лекарство остановило эффекты мутации на миграцию и ориентацию клеток, но не на общую пролиферацию стволовых клеток, что означает, что образование предракового состояния обусловлено этими первыми двумя изменениями, а не усиленной пролиферацией клеток.
Предраковые изменения в контексте Отслеживание эффектов онкогенной мутации в реальном времени в живом организме - единственный способ, которым исследователи смогли обнаружить эти принципы. Это важно, потому что рак не формируется в вакууме - он сильно зависит от своей микросреды для роста и поддержания себя. Ученым также нужно было отслеживать не только поведение отдельных клеток, но и молекул внутри этих клеток.
"Подход, который мы использовали для понимания этих онкогенных событий, действительно заключается в соединении на разных масштабах," сказала Греко. "Структура и подходы, которые использовал доктор Синь в сотрудничестве с доктором Реготом, позволили нам перейти к молекулярным элементам, связывая их с клеточным и тканевым масштабом, что дает нам разрешение на эти события, которое так трудно достичь вне живого организма."
Теперь исследователи хотят отслеживать процесс на более длительный срок, чтобы увидеть, что происходит после того, как формируется начальный бугорок. Они также хотят изучить другие онкогенные события, такие как воспаление, чтобы выяснить, применимы ли обнаруженные принципы в других контекстах.
