Новые публикации
Выявлен белок, ответственный за генетическое воспалительное заболевание
Последняя редакция: 14.06.2024

Весь контент Web2Health проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Команда исследователей под руководством доктора Хиротсугу Оды из Кластера превосходства CECAD по исследованию старения при Университете Кёльна обнаружила роль, которую играет определённый белковый комплекс в некоторых формах иммунной дисрегуляции. Этот результат может привести к разработке новых терапевтических подходов, направленных на снижение аутоинфляции и «восстановление» иммунной системы пациентов, страдающих от генетической дисфункции этого белкового комплекса.
Исследование «Biallelic human SHARPIN loss of function induces autoinflammation and immunodeficiency» было опубликовано в журнале Nature Immunology.
Линейный убиквитин-собирающий комплекс (LUBAC), состоящий из белков HOIP, HOIL-1 и SHARPIN, давно признан за свою критическую роль в поддержании иммунного гомеостаза. Предыдущие исследования на мышах показали серьёзные последствия потери SHARPIN, приводящие к тяжёлому дерматиту из-за чрезмерной гибели клеток кожи. Однако конкретные последствия дефицита SHARPIN для здоровья человека до сих пор оставались неясными.
Исследовательская группа впервые сообщила о двух людях с дефицитом SHARPIN, которые демонстрируют симптомы аутоинфляции и иммунодефицита, но неожиданно не проявляют дерматологических проблем, как это было у мышей.
При дальнейшем исследовании было обнаружено, что у этих людей нарушен канонический ответ NF-κB, важный для иммунного ответа путь. У них также была повышенная чувствительность к гибели клеток, вызванной членами суперсемейства факторов некроза опухоли (TNF). Лечение одного из пациентов с дефицитом SHARPIN анти-TNF терапией, которая специально подавляет гибель клеток, вызванную TNF, привело к полному разрешению аутоинфляции на клеточном уровне и в клиническом представлении.
Исследование показывает, что чрезмерная и неконтролируемая гибель клеток играет критическую роль в генетических воспалительных заболеваниях человека. Команда Оды добавила дефицит SHARPIN как новый член группы генетических воспалительных заболеваний человека, которые они предлагают назвать «врождёнными ошибками гибели клеток».
Защита от иммунной дисрегуляции Исследование было начато в лаборатории доктора Дэна Кастнера в Национальных институтах здравоохранения (NIH) в США. Учёные там имели возможность наблюдать одного пациента с детским началом необъяснимых эпизодов лихорадки, артрита, колита и иммунодефицита.
Получив информированное согласие, они провели экзомное секвенирование пациента и членов его семьи и обнаружили, что у пациента есть разрушительный генетический вариант в гене SHARPIN, ведущий к недетектируемым уровням белка SHARPIN. Они также выявили, что клетки пациента демонстрируют повышенную склонность к гибели как в культивируемых клетках, так и в биопсиях пациента.
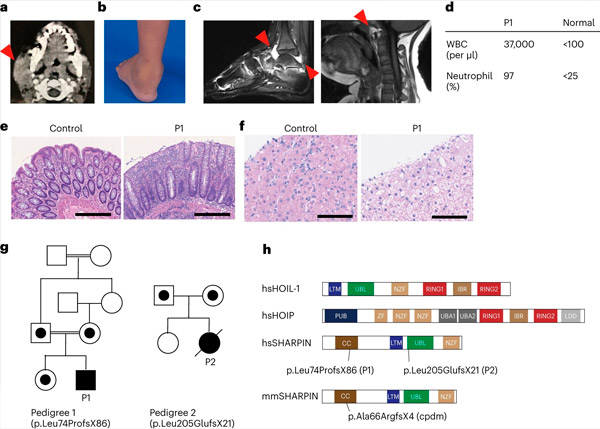
Дефицит SHARPIN у человека вызывает аутоинфламмацию и гликогеноз печени. Источник: Nature Immunology (2024). DOI: 10.1038/s41590-024-01817-w
Команда также обнаружила, что развитие лимфоидных герминальных центров — специализированных микроструктур в аденоидах, которые критически важны для созревания В-клеток нашей иммунной системы и, следовательно, для производства антител — было значительно уменьшено из-за повышенной гибели В-клеток. Эти результаты объясняют иммунодефицит у пациентов и подчеркивают важную роль LUBAC в поддержании иммунного гомеостаза у людей.
«Наше исследование подчеркивает критическую важность LUBAC в защите от иммунной дисрегуляции. Разъясняя молекулярные механизмы, лежащие в основе дефицита LUBAC, мы прокладываем путь для новых терапевтических стратегий, направленных на восстановление иммунного гомеостаза», — сказал Ода, ведущий автор исследования.
Он добавил: «Один из пациентов с дефицитом SHARPIN был зависим от инвалидного кресла в течение многих лет до того, как мы впервые его увидели. Его лодыжки были воспалены, и ходить было слишком больно. Генетический диагноз позволил нам нацелиться на правильный молекулярный путь, лежащий в основе его состояний».
С тех пор, как пациент начал получать анти-TNF терапию, он был без симптомов почти семь лет. «Как клиницист и ученый, я рад, что у меня есть возможность положительно повлиять на жизнь одного пациента благодаря нашим исследованиям», — заключил Ода.
