Медицинский эксперт статьи
Новые публикации
Амилоидоз печени
Последняя редакция: 29.06.2025

Весь контент Web2Health проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
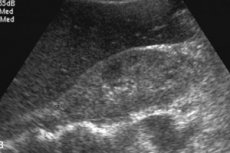
Амилоидоз обычно является системной, общей патологией, которая характеризуется накоплением амилоида (специфического гликопротеида) в тканях и последующим расстройством нормальной работы органов. Амилоидоз печени встречается значительно реже, чем почек и селезенки [1] однако практически всегда сопровождает системное поражение организма. Ни один из существующих методов визуализации не способен конкретно продемонстрировать наличие амилоида. Даже при подозрении на клинически и рентгенологически диагноз амилоидоза зависит от биопсии ткани, подтверждающей наличие отложений амилоида. [2] Лечение сложное, комплексное, включает в себя иммунодепрессивные и симптоматические мероприятия. В тяжелых случаях может потребоваться трансплантация печени.
Код по МКБ-10
Эпидемиология
Успех лечения напрямую зависит от своевременной диагностики заболевания, которое вызывает формирование в разных органах и печени белково-полисахаридного комплекса (амилоида). Как показывает практика, амилоидоз сложно предположить, или заподозрить, хотя идентифицировать и подтвердить его можно. Дело в том, что более чем в 80% нераспознанных случаев заболевание клинически маскируется под печеночную патологию. Наиболее эффективным диагностическим методом является биопсия.
Амилоидоз печени – это более редкая проблема, если сравнивать с почечным амилоидозом. При этом все случаи печеночного поражения сопровождаются поражением и других органов. Чаще всего патология затрагивает преимущественно структурные части печеночной триады, что и обусловливает минимум и неспецифичность симптоматики. Клиническая и морфологическая картина гепатоцеллюлярного дефицита и портальной гипертензии проявляется при диффузном и интралобулярном типе патологии.
Проведение печеночной биопсии оправдано, если речь идет о гепатомегалии без предшествующих печеночных симптомов и на фоне отсутствия нефротического синдрома.
Диффузное поражение печени отмечается примерно в 25% случаев, а у 75% больных поражаются лишь портальные тракты.
Первичный амилоидоз в 90% случаев поражает печень, а вторичный – лишь в 47% случаев.
Изолированное поражение печени встречается крайне редко. Обычно синхронно поражаются почки (около 93% случаев), селезенка (72%), сердце (57%), поджелудочная железа (36%), надпочечники (29%), кишечник и легкие (по 21%).
Женщины болеют почти в два раза чаще мужчин. Средняя продолжительность жизни больных амилоидозом – 52-64 года.
Причины амилоидоза печени
Амилоидоз протекает с формированием и скоплением в тканях печени сложного полисахаридно-белкового комплекса – амилоида. Проблема возникновения первичного поражения на сегодняшний день изучена недостаточно. Что касается вторичной патологии, то ее появление обычно ассоциируют с такими заболеваниями:
- хронические инфекционные процессы (туберкулез, сифилис, актиномикоз);
- гнойные воспалительные процессы (микробный эндокардит, остеомиелит, бронхоэктатическая болезнь и пр.);
- злокачественные заболевания (лейкоз, висцеральный рак, лимфогранулематоз).
Реактивная форма амилоидоза обнаруживается у пациентов с сопутствующим атеросклерозом, ревматологическими заболеваниями (болезнь Бехтерева, ревматоидный артрит), псориазом, хроническими воспалительными и мультисистемными процессами (в том числе саркоидозом). Основные факторы риска: наследственная предрасположенность, расстройства клеточного иммунитета, гиперглобулинемия.
Патогенез
Существует ряд предположений касательно происхождения амилоидоза печени. Большинство специалистов придерживаются версии диспротеиноза, иммунологической и мутационной природы заболевания, а также локального клеточного генеза. Версия клеточного генеза включает в себя изменение реакций, работающих на клеточном уровне (формирование фибриллярных прекурсоров амилоида комплексом макрофагов), хотя амилоид образуется и скапливается вне клеточных структур.
Версия диспротеиноза основывается на том, что амилоид – это продукт неправильного обмена белка. Базовое патогенетическое звено проблемы заключается в диспротеинемии и гиперфибриногенемии, которые приводят к накоплению в плазме грубодисперсных белковых и парапротеиновых фракций.
Согласно иммунологической версии, формирование амилоида обусловлено реакцией антиген-антитело, где в качестве антигенов выступает продукция тканевого распада или чужеродные белки. Амилоидные накопления обнаруживаются в основном в области образования антител и чрезмерного присутствия антигенов.
Наиболее правдоподобной версией ученые считают мутационную теорию, которая учитывает множество мутагенных факторов, способных привести к нарушениям белкового синтеза.
Амилоид – это сложный гипопротеид, который состоит из глобулярных и фибриллярных протеинов, объединенных с полисахаридами. Амилоидные скопления затрагивают интиму и адвентицию сосудистой сети, строму паренхиматозных органов, структуру желез и пр. Небольшие скопления не вызывают функциональных нарушений, а вот при интенсивном амилоидном присутствии печень увеличивается в объеме, изменяется вид органа, развивается недостаточность функции.
Печеночный амилоидоз характеризуется отложением амилоидных фибрилл в пространстве Диссе, которое обычно начинается в перипортальной области, хотя иногда оно имеет центрилобулярный характер и может также откладываться в печеночной сосудистой сети. [3], [4] В тяжелых случаях отложение амилоида приводит к давлению атрофии гепатоцитов, что препятствует прохождению желчи, что приводит к холестазу, или может блокировать синусоиды, что приводит к портальной гипертензии. [5], [6], [7]
Симптомы амилоидоза печени
Клиническая картина при амилоидозе печени многообразна, зависит от интенсивности накопления амилоида, от его биохимических особенностей, продолжительности патологического процесса, степени поражения органов и нарушения их функционального состояния.
На скрытой стадии амилоидоза, когда амилоидные накопления в печени удается обнаружить лишь при помощи микроскопического исследования, первые признаки заболевания отсутствуют. С дальнейшим развитием и нарастанием функционального дефицита органа прогрессирует и симптоматика.
Печень постепенно уплотняется, увеличивается. Методом пальпации можно прощупать измененные, но ровные и безболезненные границы органа. Редко патология сопровождается болью в подреберье с правой стороны, диспепсией, увеличением селезенки, пожелтением кожных, слизистых покровов и склер, геморрагическим синдромом.
Наиболее характерные симптомы при амилоидозе печени: [8], [9]
- накопление амилоидов в печени вызывает гепатомегалию у 33–92% пациентов;
- умеренная желтуха
- портальная гипертензия;
- холестаз от умеренной до тяжелой степени.
Так как амилоидоз крайне редко затрагивает только один орган, обычно присутствует и дополнительная симптоматика:
- при поражении почек развивается нефротический синдром и артериальная гипертензия с дальнейшей почечной недостаточностью, возникают отеки, иногда отмечается тромбоз почечных вен, обнаруживается лейкоцитурия, гематурия, гипопротеинемия, азотемия и пр.;
- при поражении сердца развивается состояние, близкое к рестриктивной кардиомиопатии (нарушения ритма, кардиомегалия, нарастающий сердечный дефицит, слабость и одышка, отечность, реже – скопление жидкости в брюшной и плевральной полости, перикардит);
- при поражении пищеварительного тракта может возникать макроглассия, слабость и расстройство перистальтики пищевода, тошнота и изжога, запоры или диарея и пр.;
- при поражении поджелудочной железы присутствует симптоматика хронического панкреатита;
- если в процесс вовлечен опорно-двигательный механизм, развивается симметричный полиартрит, туннельный синдром запястья, миопатии, а при поражении нервной системы обнаруживаются полиневропатии, параличи, ортостатическое понижение давления, повышение потоотделения, деменция.
Если патологическая реакция распространяется на кожные покровы, появляются многочисленные воскообразные бляшки на лице, шее, в кожных складках. Возможна картина нейродермита, красного плоского лишая, склеродермии.
Сочетание множественных амилоидных поражений и разнообразие симптоматики значительно усложняют идентификацию амилоидоза печени и требуют проведения комплексной и полноценной диагностики.
Формы
По классификации ВОЗ различают пять типов амилоидоза:
- AL (первичный);
- AA (вторичный);
- ATTR (наследственно обусловленный и старческий системный);
- Aβ2M (у больных на гемодиализе);
- AIAPP (у пациентов с инсулиннезависимым сахарным диабетом);
- AB (при болезни Альцгеймера);
- AANF (старческий амилоидоз предсердий).
Встречается локальный амилоидоз печени, но чаще речь идет о системном поражении, при котором в патологический процесс вовлекаются также почки, сердце, селезенка, нервная система, а также другие органы и ткани.
Осложнения и последствия
Системный амилоидоз постепенно приводит к развитию острых патологических процессов, способных, в свою очередь, привести к летальному исходу. Среди наиболее распространенных и жизнеугрожающих осложнений можно назвать следующие:
- учащающиеся инфекционные (бактериальные, вирусные) патологии, в том числе пневмонии, пиелонефриты, гломерулонефриты;
- хроническая печеночная и почечная недостаточность;
- хроническая сердечная недостаточность (может предшествовать инфаркт миокарда);
- геморрагические инсульты.
Тромбозы вен происходят в результате накопления и оседания белков на венозных стенках. Просвет пораженных сосудов сужается, развивается органная недостаточность. Со временем на фоне длительно существующей гиперпротеинемии сосуд может полностью перекрываться. Любое из осложнений способно привести к неблагоприятному финалу – летальному исходу.
Диагностика амилоидоза печени
При подозрении амилоидоза печени диагностические мероприятия проводят после обязательных консультаций, как гастроэнтеролога и терапевта, так и ревматолога, кардиолога, дерматолога, невролога, уролога. Важно всесторонне оценивать данные анамнеза и клинические проявления, провести комплексную лабораторную и инструментальную диагностику.
Анализы обязательно включают в себя исследование мочи и крови. При амилоидозе печени часто обнаруживают сочетание лейкоцитурии с протеинурией и цилиндрурией, а гипопротеинемии – с гиперлипидемией, анемией, гипонатриемией и гипокальциемией, сниженным показателем тромбоцитов. В ходе электрофореза мочи и сыворотки крови обнаруживают парапротеины.
Инструментальная диагностика включает в себя:
- электрокардиограмму, ЭхоКГ;
- ультразвуковое исследование органов брюшной полости;
- рентген желудка, пищевода;
- ирригографию, рентген с барием;
- эндоскопию.
Рентгенологические данные об амилоидозе печени включают неспецифическую гепатомегалию, повышенную эхогенность при ультразвуковом исследовании или плотность при компьютерной томографии (КТ), а также увеличение интенсивности сигнала Т1 при магнитно-резонансной томографии (МРТ). [10] Сцинтиграфия со связанными с Tc-99m индикаторами показывает гетерогенное поглощение, но оно неспецифично. [11], [12] Было показано, что ГК увеличивает жесткость печени, измеренную с помощью эластографии; [13], [14], [15] однако имеется несколько сообщений об отдельных случаях. Магнитно-резонансная эластография (MRE) в настоящее время является наиболее точным неинвазивным методом выявления и определения стадии фиброза печени, [16], [17] MRE полезен для выявления прогрессирования, ответа на лечение и прогнозирования печеночной декомпенсации у пациентов с фиброзом печени. [18]
Амилоидоз печени на УЗИ определить сложно: определяется увеличение органа, при этом наиболее специфична гепатомегалия, превышающая 15 см. Под контролем УЗИ выполняют биопсию, что и становится определяющим показателем для постановки диагноза. При помощи специальной иглы отбирают небольшое количество ткани печени, затем ее окрашивают специальным красящим веществом и рассматривают под микроскопом, что позволяет непосредственно увидеть амилоидные отложения.
Окончательный диагноз ставят только после выявления амилоидных фибрилл в ткани печени и других органов. Генетически обусловленный тип амилоидоза определяют путем тщательного генно-медицинской экспертизы родословной.
Дифференциальная диагностика
Амилоидоз следует заподозрить у всех пациентов с сочетанием почечной протеинурии, рестриктивной кардиомиопатии, автономной или периферической невропатии, гепатомиелии, даже при условии отсутствия моноклонального парапротеина. Верифицировать тип амилоидоза очень важно, поскольку лечение поражений разной этиологии сильно отличается.
Гистологическая диагностика предполагает окрашивание конго-красным с последующим микроскопическим исследованием в поляризующем свете. Целесообразно проводить биопсию сразу нескольких образцов тканей. Если результат окраски становится положительным, то выполняют иммуногистохимический анализ с применением моноклональных антител к предшествующим белкам для идентификации типа амилоида.
Для дифференциации первичного амилоидоза и разных вариаций генетически обусловленного амилоидоза проводят анализ ДНК. Возможно выделение амилоидных фибрилл из биоптата и секвестрация на отдельные аминокислоты.
Дополнительные исследования для определения плазмоклеточной дискразии:
- электрофорез сывороточных белков крови и мочи;
- иммунологическое исследование на свободные легкие цепи;
- иммунофиксация (иммуноблоттинг) сывороточных белков;
- аспирация и трепанобиопсия костного мозга.
Диагностика амилоидоза печени является продолжительным и трудоемким процессом, который требует повышенной внимательности специалистов и качественного оснащения клиник и лабораторий.
К кому обратиться?
Лечение амилоидоза печени
Лечебные мероприятия нацеливают на снижение концентрации в крови предшествующих белков амилоида (устраняют причину амилоидоза) и поддержку адекватного функционирования печени.
Вторичный амилоидоз требует блокировки воспалительного процесса (при хронических инфекционных и аутоиммунных патологиях). При аутоиммунных заболеваниях рекомендуется применение цитостатиков. Для устранения хронических инфекционных процессов зачастую хирургическим путем удаляют зону воспаления. Зачастую такой подход позволяет остановить дальнейшее прогрессирование амилоидоза и улучшить функцию печени.
Первичный амилоидоз требует применения химиопрепаратов, иногда – трансплантации костного мозга.
Современные руководства рекомендуют комбинацию циклофосфамида, бортезомиба, дексаметазона (CyBorD) и даратумумаба в качестве терапии первой линии у пациентов, у которых впервые диагностирован АЛ.
Бортезомиб – ингибитор протеасом. Протеасомы участвуют в снижении протеотоксичности и регуляции белков, которые контролируют клеточную прогрессию и апоптоз. Плазматические клетки, генерирующие амилоид, особенно чувствительны к ингибированию протеасом, поскольку они полагаются на протеасому для уменьшения токсического воздействия легких цепей и предотвращения апоптоза.
Даратумумаб представляет собой моноклональное антитело (мАТ), которое связывается с CD38, трансмембранным гликопротеином, экспрессируемым на поверхности плазматических клеток, вызывая апоптоз. Это единственный препарат, специально одобренный для лечения AL-амилоидоза при применении с CyBorD. Эффективность CyBorD-даратумумаба очень высока: у 78% пациентов достигается значительный гематологический ответ (определяемый как полный ответ или очень хороший частичный ответ). Медиана выживаемости в небольшой группе пациентов, получавших CyBorD ( n = 15), составила 655 дней по сравнению со 178 днями для пациентов, получавших другое лечение на основе мелфалан-дексаметазон ( n = 10). 4
Однако эти методы лечения имеют многочисленные побочные эффекты, включая кардиотоксичность, что приводит к необходимости снижения дозы или приостановки лечения, а также использования других менее эффективных, но более переносимых терапевтических стратегий.
Исатуксимаб, моноклональные антитела против CD38, аналогичные даратумумабу, изучаются для лечения дискразии плазматических клеток, лежащей в основе АЛ.
В настоящее время изучаются три моноклональных антитела биртамимаб, CAEL-101 и AT-03, направленные на удаление амилоидных фибрилл из пораженных органов. Результаты этих исследований смогут предложить прямое доказательство гипотезы о том, что путем удаления фибрилл отложения легких цепей из органов происходит улучшение их функции. [19]
Для того чтобы поддержать работоспособность печени, назначают лекарственные средства на основе урсо-дезоксихолевой кислоты (пример – Урсосан). Урсо-дезоксихолевая кислота помогает стабилизировать мембраны клеток, снижает неблагоприятное влияние токсических жирных кислот при желчном застое, спровоцированном амилоидными отложениями, а также способствует восстановлению нормального оттока желчи.
Дополнительно назначается симптоматическая терапия и поддержка функционирования других жизненно-важных структур: нервной системы, сердца, почек и пр. Поддерживающая терапия больных амилоидозом печени включает в себя различные клинические аспекты, включая лечение сердечной недостаточности, аритмий, нарушений проводимости, тромбоэмболии и сопутствующего наличия аортального стеноза.
Другие методы лечения зависят от типа амилоидоза и от того, какие части тела поражены. Лечение может включать: [20]
- лекарства, облегчающие симптомы, такие как обезболивающие, лекарства от тошноты или лекарства, уменьшающие отек (диуретики);
- лекарства для уменьшения количества амилоида;
- диализ почек;
- трансплантация печени.
Печень производит 95% TTR (транстиретина - белок, участвующий в транспорте тироксина (Т4) и ретинол-связывающего белка. Транстиретин в основном синтезируется в печени и богат бета-нитями, которые имеют тенденцию агрегироваться в нерастворимые амилоидные фибриллы), измеренного в сыворотке. Поэтому трансплантация печени исторически (с 1990 г.) предлагалась в качестве терапии первой линии для устранения основного источника амилоидогенного TTR у пациентов при семейной форме (ATTRv), тогда как при форме ATTR-wt она не показана. Трансплантация печени молодым пациентам на ранних стадиях заболевания связана с высокой 20-летней выживаемостью. Трансплантация печени, по-видимому, более эффективна при некоторых мутациях и менее эффективна при других, таких как V122I (связанная с кардиомиопатией). Комбинированная трансплантация печени и сердца также возможна у молодых пациентов с ATTRv с кардиомиопатией, и данные литературы о небольшой группе пациентов позволяют предположить, что эта комбинация имеет лучший прогноз, чем только трансплантация сердца.
Пациентам с амилоидозом печени противопоказан прием сердечных гликозидов и антагонистов кальция типа Дилтиазема или Верапамила, способных скапливаться в амилоиде. Препараты ингибиторы АПФ и бета-адреноблокаторы используют с осторожностью.
При ортостатической гипотензии назначают минералокортикоиды, либо глюкокортикостероидные препараты, с учетом того, что они способны вызвать декомпенсацию сердечной недостаточности. Осторожно применяют и альфа-адреномиметик мидодрин (Гутрон).
При невропатиях уместно применение антиконвульсантов и антидепрессантов.
В ряде случаев амилоидоза печени врачам приходится рассматривать проведение трансплантации органа.
Профилактика
Ввиду недостатка сведений о патогенезе амилоидоза печени, специалисты не могут разработать специфическую профилактику заболевания. Поэтому основные усилия сводятся к своевременному выявлению и лечению любых хронических патологий, способных спровоцировать развитие нарушения. Если в роду имеются случаи амилоидоза любой локализации, рекомендуется систематически посещать врачей для проведения диспансерных осмотров.
В целом, профилактические мероприятия сводятся к своевременному устранению инфекционных заболеваний, особенно таких, которые имеют склонность к трансформации в хронический процесс. Речь идет о предупреждении развития туберкулеза, легочных инфекций и т. д. Немаловажно своевременное выявление и адекватное лечение стрептококковых инфекций, которые могут становиться причинами хронических форм аутоиммунных воспалительных процессов. Речь идет о скарлатине, стрептококковом тонзиллите и т. п.
Если у пациента уже присутствует аутоиммунное заболевание, то он должен систематически консультироваться с врачом, наблюдать за активностью патологии, применять необходимые медикаменты по назначению доктора, по показаниям корректировать дозировки.
Прогноз
Прогноз для пациентов с амилоидозом печени неблагоприятный. Заболевание нарастает медленно, но непрерывно, что со временем вызывает нарушение функции пораженных органов и летальный исход – в частности, обусловленной органной недостаточностю.
Больные системной патологией в основном погибают в результате развития хронической почечной недостаточности, хотя в некоторых случаях гемодиализ или постоянный амбулаторный перитонеальный диализ улучшает прогноз таких пациентов. Показатель выживаемости больных при выполнении гемодиализа, вне зависимости от его типа, можно сопоставить с выживаемостью людей, страдающих другими системными патологиями и сахарным диабетом.
Основная причина летального исхода при выполнении гемодиализа – это развитие осложнений со стороны сердечно-сосудистой системы.
Одним из основных методов лечения заболевания долгое время считалась трансплантация печени, при этом наиболее оптимистичные показатели выживаемости отмечаются у больных, возраст которых не превышает 50 лет (при условии непродолжительно существующего патологического процесса, нормального индекса массы тела). Несколько худший прогноз имеют больные, у которых амилоидоз печени сочетается с периферической невропатией.

