Медицинский эксперт статьи
Новые публикации
Причины и патогенез дифтерии
Последняя редакция: 04.07.2025

Весь контент Web2Health проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Дифтерия - это парадигма токсигенных инфекционных заболеваний. В 1883 году Клебс продемонстрировал, что Corynebacterium diphtheriae является возбудителем дифтерии. Годом позже Леффлер обнаружил, что этот организм можно культивировать только из носоглоточной полости, и предположил, что повреждение внутренних органов произошло из-за растворимого токсина. К 1888 году Ру и Йерсен показали, что у животных, которым вводили стерильные фильтраты C. diphtheriae, развивалась патология органов, неотличимая от таковой при дифтерии человека; это продемонстрировало, что сильный экзотоксин был основным фактором вирулентности.
Дифтерия - это чаще всего инфекция верхних дыхательных путей, вызывающая жар, боль в горле и недомогание. Толстая серо-зеленая фибриновая мембрана, псевдомембрана, часто образуется на участке (ах) инфекции в результате комбинированного воздействия роста бактерий, выработки токсинов, некроза подлежащей ткани и иммунного ответа хозяина. Признание того, что системное поражение органов происходит из-за действия токсина дифтерии, привело к разработке как эффективной терапии на основе антитоксина для лечения острой инфекции, так и высокоэффективной токсоидной вакцины.
Хотя иммунизация анатоксинами сделала дифтерию редким заболеванием в тех регионах, где стандарты общественного здравоохранения требуют вакцинации, вспышки дифтерии все еще происходят в неиммунизированных группах и группах с ослабленным иммунитетом. В отличие от этого, широко распространенные вспышки дифтерии, достигающие масштабов эпидемии, наблюдались в тех регионах, где были приостановлены активные программы иммунизации.
Другие виды коринебактерий
Помимо C. diphtheriae, C. ulcerans и C. pseudotuberculosis, C. pseudodiphtheriticum и C. xerosis могут иногда вызывать инфекцию носоглотки и кожи. Последние два штамма узнаваемы по их способности продуцировать пиразинамидазу. В ветеринарии C. renale и C. kutscheri являются важными патогенами и вызывают пиелонефрит у крупного рогатого скота и латентные инфекции у мышей, соответственно.
Причина
Возбудитель дифтерии - Corynebacterium diphtheriae - тонкая, слегка изогнутая палочка с булавовидными утолщениями на концах, неподвижная; спор, капсул и жгутиков не образует, грамположительна.
Кроме токсина, коринебактерии дифтерии в процессе жизнедеятельности продуцируют нейраминидазу, гиалуронидазу, гемолизин, некротизирующий и диффузный факторы, способные вызвать некроз и разжижение основного вещества соединительной ткани.
По способности образовывать токсин коринебактерии дифтерии подразделяют на токсигенные и нетоксигенные.
Дифтерийный токсин - сильнодействующий бактериальный экзотоксин - определяет как общие, так и местные клинические проявления болезни. Токсигенность генетически детерминирована. Нетоксигенные коринебактерии дифтерии заболевания не вызывают.
По культуральным и морфологическим особенностям все коринебактерии дифтерии делят на 3 варианта: gravis, mitis, intermedius. Прямой зависимости тяжести заболевания от варианта коринебактерии дифтерии нет. Каждый вариант содержит как токсигенные, так и нетоксигенные штаммы. Токсигенные коринебактерии всех вариантов продуцируют идентичный токсин. [1]
Структура, классификация и антигенные типы
Corynebacterium diphtheriae - это грамположительная неподвижная булавовидная палочка. Штаммы, растущие в ткани, или более старые культуры in vitro содержат тонкие пятна в клеточных стенках, которые позволяют обесцвечивать во время окрашивания по Граму и приводят к реакции с переменной Грамом. Более старые культуры часто содержат метахроматические гранулы (полиметафосфат), которые окрашиваются в голубовато-пурпурный цвет с помощью метиленового синего. Сахара клеточной стенки включают арабинозу, галактозу и маннозу. Кроме того, может быть выделен токсичный 6,6'-сложный эфир трегалозы, содержащий коринемиколиновую и коринемиколеновую кислоты в эквимолярных концентрациях. Выделяются три различных культурных типа: mitis, intermedius, gravis.
Большинству штаммов для роста необходимы никотиновая и пантотеновая кислоты; некоторым также требуется тиамин, биотин или пимелиновая кислота. Для оптимального производства токсина дифтерии среда должна быть дополнена аминокислотами и должна быть отложена.
Еще в 1887 году Лёффлер описал выделение авирулентных (нетоксигенных) дифтерий C., которые были неотличимы от вирулентных (токсигенных) штаммов, выделенных от пациентов, у здоровых людей. В настоящее время признано, что авирулентные штаммы C. diphtheriae могут быть преобразованы в вирулентный фенотип после инфицирования и лизогенизации одним из ряда отдельных коринебактериофагов, несущих структурный ген токсина дифтерии, tox. Лизогенное преобразование авирулентного фенотипа в вирулентное может происходить как in situ, так и in vitro. Структурный ген дифтерийного токсина не является существенным ни для коринебактериофага, ни для C. diphtheriae.. Несмотря на это наблюдение, генетический дрейф токсина дифтерии не наблюдался.
Патогенез
Входные ворота инфекции - слизистые оболочки ротоглотки, носа, гортани, реже - слизистая оболочка глаз и половых органов, а также повреждённая кожа, раневая или ожоговая поверхность, опрелости, незажившая пупочная ранка. В месте входных ворот коринебактерия дифтерии размножается и выделяет экзотоксин.
Происходят выпотевание экссудата, богатого фибриногеном, и превращение его в фибрин под влиянием тромбокиназы, освободившейся при некрозе эпителиальных клеток. Образуется фибринозная плёнка - характерный признак дифтерии.
Бессимптомное носоглоточное носительство распространено в регионах, эндемичных по дифтерии. У восприимчивых людей токсигенные штаммы вызывают заболевание, размножая и выделяя дифтерийный токсин в носоглотке или поражениях кожи. Дифтерийное поражение часто покрыто псевдомембраной, состоящей из фибрина, бактерий и воспалительных клеток. Токсин дифтерии может быть протеолитически расщеплен на два фрагмента: N-концевой фрагмент A (каталитический домен) и фрагмент B (трансмембранный и рецепторсвязывающий домены). Фрагмент А катализирует НАД + -зависимое АДФ-рибозилирование фактора элонгации 2, тем самым подавляя синтез белка в эукариотических клетках. Фрагмент B связывается с рецептором клеточной поверхности и облегчает доставку фрагмента A в цитозоль.
Защитный иммунитет включает реакцию антител на дифтерийный токсин после клинического заболевания или на дифтерийный токсин (токсин, инактивированный формальдегидом) после иммунизации.
Колонизация
Мало что известно о факторах колонизации C. diphtheriae. Однако очевидно, что факторы, помимо выработки дифтерийного токсина, способствуют вирулентности. Эпидемиологические исследования показали, что данный лизотип может сохраняться в популяции в течение длительных периодов времени. Позже он может быть заменен другим лизотипом. Возникновение и последующее преобладание нового лизотипа в популяции предположительно связано с его способностью колонизировать и эффективно конкурировать в своем сегменте экологической ниши носоглотки. Corynebacterium diphtheriae может продуцировать нейраминидазу, которая расщепляет сиаловую кислоту с поверхности клетки на ее компоненты пируват и N-ацетилнейраминовую кислоту. Корд-фактор (6,6'-ди-O-миколоил-α, α'-D-трегалоза) является поверхностным компонентом C. diphtheriae, но его роль в колонизации человеческого хозяина неясна.
Производство токсинов дифтерии
Структурный ген токсина дифтерии, tox, принадлежит семейству близкородственных коринебактериофагов, из которых β-фаг наиболее изучен. Регуляция экспрессии дифтерийного токсина опосредуется репрессором, активируемым железом, DtxR, который кодируется геномом C. diphtheriae. Выражение токсина зависит от физиологического состояния C. diphtheriae. В условиях, в которых железо становится роста ограничение скорости подложки, железа диссоциирует от DtxR, то токсикодендрон ген становится активируются, и дифтерийный токсин синтезируется и секретируется в культуральную среду при максимальных скоростей.
Токсин дифтерии необычайно мощный; для чувствительных видов (например, людей, обезьян, кроликов, морских свинок) всего от 100 до 150 нг / кг массы тела является летальным. Токсин дифтерии состоит из одной полипептидной цепи из 535 аминокислот. Биохимический генетический и рентгеноструктурный анализ показывают, что токсин состоит из трех структурных / функциональных доменов:
- N-концевой АДФ-рибозилтрансферазы (каталитический домен);
- область, которая облегчает доставку каталитического домена через клеточную мембрану (трансмембранный домен);
- домен связывания рецептора эукариотических клеток.
После мягкого переваривания трипсином и восстановления в денатурирующих условиях дифтерийный токсин может быть специфически расщеплен в его чувствительной к протеазе петле на два полипептидных фрагмента (A и B). Фрагмент A представляет собой N-концевой компонент токсина 21 кДа и содержит каталитический центр ADP-рибозилирования фактора элонгации 2 (EF-2)
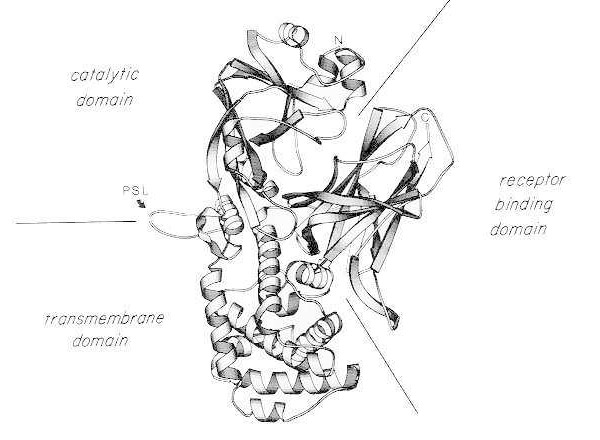
Ленточная диаграмма рентгеновской кристаллической структуры мономерного нативного дифтерийного токсина. (модифицировано из Bennett MJ, Choe S, Eisenberg D: Domain swapping: Entangling aliances между белками. Proc Natl Acad Sci, USA, 91: 3127, 1994). Показаны относительные положения каталитического, трансмембранного и рецептор-связывающего доменов. Интактный токсин может расщепляться трипсиноподобными протеазами на Arg190, Arg192 и / или Arg193, которые расположены в чувствительной к протеазе петле (PSL). После восстановления дисульфидного мостика между Cys186 и Cys201 токсин может быть разделен на фрагменты A и B. Показаны аминоконце (N) и карбокси-конец (C) интактного токсина. Ленточная диаграмма была создана с помощью программы MOLESCRIPT.
С-концевой фрагмент, фрагмент B, несет трансмембранный и рецепторсвязывающий домены токсина.
Отравление одиночной эукариотической клетки дифтерийным токсином включает, по крайней мере, четыре различных этапа:
- связывание токсина с его рецептором на клеточной поверхности;
- кластеризация заряженных рецепторов в покрытые ямки и интернализация токсина посредством рецептор-опосредованного эндоцитоза; после подкисления эндоцитарной везикулы с помощью ассоциированного с мембраной, управляемого АТФ протонного насоса,
- встраивание трансмембранного домена в мембрану и облегченная доставка каталитического домена в цитозоль, и
- АДФ-рибозилирование EF-2, что приводит к необратимому подавлению синтеза белка.
Было показано, что одной молекулы каталитического домена, доставленной в цитозоль, достаточно, чтобы быть летальным для клетки.
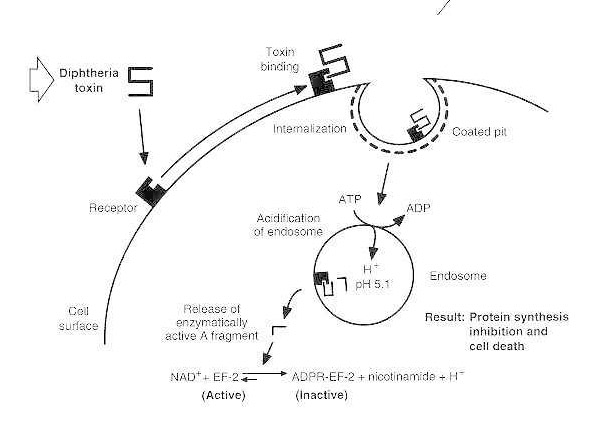
Схематическая диаграмма дифтерийной интоксикации чувствительной эукариотической клетки.
Токсин связывается со своим рецептором на клеточной поверхности и интернализуется посредством рецептор-опосредованного эндоцитоза; при подкислении эндосомы трансмембранный домен встраивается в мембрану везикул; каталитический домен доставляется в цитозоль, что приводит к ингибированию синтеза белка и гибели клетки.
Эпидемиология
До массовой иммунизации населения США анатоксином дифтерии дифтерия обычно была детской болезнью. Замечательный аспект массовой иммунизации дифтерийным анатоксином заключается в том, что по мере увеличения процента населения с защитным уровнем антитоксинового иммунитета (≥ 0,01 МЕ / мл) частота выделения токсигенных штаммов из популяции уменьшается. Сегодня в Соединенных Штатах, где наблюдается почти полное исчезновение клинической дифтерии, выделение токсигенных штаммов C. diphtheriaeредко. Поскольку субклиническая инфекция больше не является источником воздействия дифтерийного антигена и, если ее не усилить, иммунитет к антитоксину ослабевает, большой процент взрослых (от 30 до 60%) имеют уровни антитоксина ниже защитного уровня и находятся в группе риска. В США, Европе и Восточной Европе недавние вспышки дифтерии произошли в основном среди лиц, злоупотребляющих алкоголем и / или наркотиками. Внутри этой группы носители токсигенных C diphtheriae имеют умеренно высокий уровень антитоксического иммунитета. Недавний срыв мер общественного здравоохранения в России привел к тому, что дифтерия стала эпидемией. К концу 1994 г. в России было зарегистрировано более 80 000 случаев заболевания и более 2 000 смертей.
Очаговые вспышки дифтерии почти всегда связаны с иммунным носителем, который вернулся из региона, где дифтерия является эндемической. Действительно, недавние вспышки клинической дифтерии в США и Европе были связаны с путешественниками, возвращающимися из России и Восточной Европы. Токсигенные штаммы C. diphtheriae передаются напрямую от человека к человеку путем воздушно-капельной инфекции. Известно, что токсигенные штаммы могут непосредственно колонизировать носоглоточную полость. Кроме того, токсический ген может распространяться косвенно путем высвобождения токсигенного коринебактериофага и лизогенного преобразования нетоксигенных автохтонных C diphtheriae in situ. [5]
В дополнение к определению биотипа и лизотипа изолятов C. diphtheriae теперь можно использовать молекулярно-биологические методы при изучении вспышек дифтерии. При изучении клинических вспышек заболевания использовались паттерны переваривания рестрикционной эндонуклеазой хромосомной ДНК C. diphtheriae, а также использование клонированных последовательностей вставок коринебактерий в качестве генетического зонда.
Тест Шика использовался в течение многих лет для оценки иммунитета к дифтерийному токсину, хотя сегодня он был заменен во многих регионах серологическим тестом на специфические антитела к дифтерийному токсину. В тесте Шика небольшое количество дифтерийного токсина (примерно 0,8 нг в 0,2 мл) вводится внутрикожно в предплечье (тестируемый участок) и 0,0124 мкг дифтерийного токсина в 0,2 мл вводится внутрикожно в контрольный участок. Через 48 и 96 часов снимают показания. Неспецифические кожные реакции обычно достигают максимума через 48 часов. Через 96 часов эритематозная реакция с некоторым возможным некрозом на участке тестирования указывает на недостаточный антитоксический иммунитет для нейтрализации токсина (≤ 0,03 МЕ / мл). Воспаление как в исследуемом, так и в контрольном участках через 48 часов указывает на реакцию гиперчувствительности на препарат антигена.
Формы
Corynebacterium diphtheriae поражает носоглотку или кожу. Токсигенные штаммы выделяют сильный экзотоксин, который может вызвать дифтерию. Симптомы дифтерии включают фарингит, лихорадку, отек шеи или области вокруг поражения кожи. Дифтерийные поражения покрыты псевдомембраной. Токсин распространяется по кровеносной системе в отдаленные органы и может вызвать паралич и застойную сердечную недостаточность. [6]
Выделяют два типа клинической дифтерии: носоглоточную и кожную. Симптомы дифтерии глотки варьируются от легкого фарингита до гипоксии из-за обструкции дыхательных путей псевдомембраной. Поражение шейных лимфатических узлов может вызвать сильный отек шеи (дифтерия бычьей шеи), и у пациента может возникнуть лихорадка (≥ 103 ° F). Поражения кожи при кожной дифтерии обычно покрываются псевдомембраной серо-коричневого цвета. В результате действия дифтерийного токсина на периферические двигательные нейроны и миокард могут развиться опасные для жизни системные осложнения, в основном потеря двигательной функции (например, затруднение глотания) и застойная сердечная недостаточность.
Контроль
Борьба с дифтерией зависит от адекватной иммунизации дифтерийным анатоксином: инактивированным формальдегидом дифтерийным токсином, который остается нетронутым с антигенной точки зрения. Анатоксин получают инкубацией дифтерийного токсина с формальдегидом при 37 ° C в щелочных условиях. Иммунизацию против дифтерии следует начинать на втором месяце жизни с серии из трех первичных доз с интервалом от 4 до 8 недель, за которыми следует четвертая доза примерно через 1 год после последней первичной прививки. Дифтерийный анатоксин широко используется в качестве компонента вакцины АКДС (дифтерия, коклюш, столбняк). Эпидемиологические исследования показали, что иммунизация против дифтерии эффективна примерно на 97%. Хотя массовая иммунизация против дифтерии практикуется в Соединенных Штатах и Европе, и уровень иммунизации детей достаточен, большая часть взрослого населения может иметь титры антител ниже защитного уровня. Взрослое население следует повторно вакцинировать дифтерийным анатоксином каждые 10 лет. Действительно, бустерная иммунизация дифтерийно-столбнячным анатоксином должна проводиться лицам, путешествующим в регионы с высокими показателями эндемической дифтерии (Центральная и Южная Америка, Африка, Азия, Россия и Восточная Европа). В последние годы использование высокоочищенных препаратов токсоидов для иммунизации свело к минимуму случайные тяжелые реакции гиперчувствительности. бустерная иммунизация дифтерийно-столбнячным анатоксином должна проводиться лицам, путешествующим в регионы с высокими показателями эндемической дифтерии (Центральная и Южная Америка, Африка, Азия, Россия и Восточная Европа). В последние годы использование высокоочищенных препаратов токсоидов для иммунизации свело к минимуму случайные тяжелые реакции гиперчувствительности. бустерная иммунизация дифтерийно-столбнячным анатоксином должна проводиться лицам, путешествующим в регионы с высокими показателями эндемической дифтерии (Центральная и Южная Америка, Африка, Азия, Россия и Восточная Европа). В последние годы использование высокоочищенных препаратов токсоидов для иммунизации свело к минимуму случайные тяжелые реакции гиперчувствительности.
Хотя антибиотики (например, пенициллин и эритромицин) используются как часть лечения пациентов с дифтерией, быстрая пассивная иммунизация дифтерийным антитоксином наиболее эффективна для снижения летальности. Длительный период полураспада специфического антитоксина в кровотоке является важным фактором в обеспечении эффективной нейтрализации дифтерийного токсина; однако, чтобы быть эффективным, антитоксин должен вступить в реакцию с токсином, прежде чем он попадет в клетку.
Модернизация дифтерийного токсина для разработки эукариотических рецепторно-специфических цитотоксинов
Белковая инженерия - новая и быстро развивающаяся область в области молекулярной биологии; он объединяет методологии рекомбинантной ДНК и твердофазный синтез ДНК для разработки и конструирования химерных генов, продукты которых обладают уникальными свойствами. Изучение взаимосвязей между структурой и функцией дифтерийного токсина ясно показало, что этот токсин представляет собой трехдоменный белок: каталитический, трансмембранный и рецепторный. Было возможно генетически заменить нативный домен, связывающий рецептор дифтерийного токсина, различными полипептидными гормонами и цитокинами (например, гормоном, стимулирующим α-меланоциты [α-MSH], интерлейкином (IL) 2, IL-4, IL- 6, ИЛ-7, фактор роста эпидермиса). Полученные химерные белки или слитые токсины сочетают рецептор-связывающую специфичность цитокина с трансмембранным и каталитическим доменами токсина. В каждом случае было показано, что слитые токсины избирательно отравляют только те клетки, которые несут соответствующий целевой рецептор. Первый из этих генетически модифицированных токсинов слияния, DAB 389IL-2 в настоящее время оценивается в клинических испытаниях на людях для лечения резистентных лимфом и аутоиммунных заболеваний, при которых клетки с высокоаффинными рецепторами IL-2 играют важную роль в патогенезе. [7] Было показано, что введение DAB 389 IL-2 безопасно, хорошо переносится и способно вызывать стойкую ремиссию заболевания при отсутствии серьезных побочных эффектов. Вероятно, что гибридные токсины на основе дифтерийного токсина станут важными новыми биологическими агентами для лечения конкретных опухолей или заболеваний, при которых могут быть нацелены специфические рецепторы клеточной поверхности.


 [
[