Медицинский эксперт статьи
Новые публикации
Биопсия и гистология шейки матки при дисплазии
Последняя редакция: 04.07.2025

Весь контент Web2Health проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
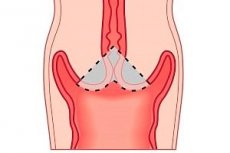
Биопсия - это слово пугает многих женщин, хотя сама процедура не представляет собой опасности. Тревожить может только ее результат, который далеко не всегда бывает плохим. Биопсия шейки матки при дисплазии скорее предназначена для исключения риска развития онкологии и является одной из самых распространенных процедур в комплексном обследовании женщин.
Описание процедуры, как происходит биопсия шейки матки при дисплазии?
- Биопсия – это забор небольшого количества ткани эпителия для изучения.
- В процедуре используется очень тонкая специальная игла с полостью.
- Биопсию проводят во время кольпоскопического осмотра.
- Игла вводится в эпителиальную ткань после нанесения местного анестетика.
- Полученный биоптат (материал) пересылается в лабораторию для гистологического исследования.
- Клеточный материал подвергается специальной обработке (окрашиванию) и исследуется под микроскопом.
- Гистология позволяет определить, насколько дисплазия шейки матки опасна. Оценивается сохранность структуры клеток, их морфология, количество слоев ткани.
- Анализ позволяет определить степень поражения эпителиальной ткани и уточнить предварительный диагноз.
Биопсия считается высокоинформативным методом, плюс этой процедуры в том, что она практически безболезненная и относится к малоинвазивным методам обследования
Гистология при дисплазии шейки матки
Гистологические исследования входят в комплекс диагностики, если гинеколог на первичном осмотре обнаружил у женщины дисплазию шейки матки. Именно гистология дает возможность уточнить диагноз, исключить или подтвердить рак, карциному.
Рассмотрим подробнее, что такое гистология:
- Гистологией называют метод, который изучает строение ткани, выявляет все отклонения в клеточной структуре.
- Основа гистологии - исследование среза тканевого материала, в данном случае - эпителия шейки матки.
- Отличие гистологии и цитологии заключается в том, что при биопсии проводится более глубокий забор материала. Цитология предполагает соскоб с поверхности эпителия шейки.
- Гистологию проводят вовремя кольпоскопического осмотра. Чаще всего после первичной кольпоскопии, которая и определяет участок забора биоптата.
- Гистологическое исследование не считается сложным, исключение - случаи, когда поражение эпителия не выражено явно и требуется провести несколько биопсий с разных секторов шейки матки
- Полученный биоптат исследуют с помощью окрашивания. В норме эпителиальная ткань показывает после окрашивания коричневый цвет. Если есть патологические изменения, окрас ткани меняется слабо или же материал вовсе не меняет цвет.
- При проведении гистологии ткань шейки повреждается, чтобы избежать инфицирования или кровотечения, участок может ушиваться. Но чаще всего после биопсии применяют стерильный кровоостанавливающий тампон, который вполне справляется с функцией защиты и регенерации ткани.
Какими методами может проводиться гистология?
- Стандартная биопсия с помощью специальной полой иглы.
- Иссечение небольшого участка ткани с помощью специального медицинского электроножа (диатермоэкцизия).
- Лазерная эксцизия.
- Иссечение с помощью новейшего современного инструмента - радионожа.
- Забор ткани с помощью скальпеля.
Рекомендации для гистологического забора ткани
- Это наименее травматичный и подходящий метод для молодых, нерожавших женщин.
- Если предполагаемый измененный участок эпителия невелик, в любом секторе шейки забор проводят щадящим способом.
- Для гистологии обязательны предварительные диагностические процедуры - осмотр, цитология, кольпоскопия.
Нормальные результаты гистологии не исключают необходимость регулярных осмотров и диагностики. Посещение гинеколога хотя бы один раз в год должно быть нормой для каждой здравомыслящей женщины, поскольку дисплазия шейки матки может развиваться бессимптомно и без характерных признаков.
По каким критериям определяется диагноз после биопсии?
- Если есть нарушения в структуре слоев эпителия.
- Когда наружный слой показывает активность созревания клеток (увеличение рибосом).
- Если определяется снижение синтеза специфичного гликогена.
- Контактность клеток (десмос) снижена.
- Ядро клетки подвержено патологическим изменениям.
- Явно видимые атипичные митохондрии, другие нестандартные составляющие ДНК клетки.
- Изменения клеточной формы (цилиндрические).
Степень нарушения клеток эпителия:
- Первая – фоновые изменения, выражены слабо.
- Умеренная, вторая степень – атипичные изменения выражены в половине всех слоев.
- Выраженная атипия, третья степень – изменения коснулись двух и более слоев эпителия.


 [
[