Медицинский эксперт статьи
Новые публикации
Лечение тяжелого сепсиса и септического шока
Последняя редакция: 23.04.2024

Весь контент Web2Health проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Эффективное лечение сепсиса возможно только при условии полноценной хирургической санации очага инфекции и адекватной антимикробной терапии. Неадекватная стартовая антимикробная терапия - фактор риска летального исхода у больных с сепсисом. Поддержание жизни больного, предотвращение и устранение органных дисфункций возможны только при целенаправленной интенсивной терапии.
Основная её цель - оптимизация транспорта О2 в условиях его повышенного потребления, что характерно для тяжелого сепсиса и септического шока. Данное направление лечения реализуют посредством гемодинамической и респираторной поддержки.
Гемодинамическая поддержка
Инфузионная терапия
Инфузионная терапия - одно из первоначальных мероприятий поддержания гемодинамики и прежде всего СВ. Ее основные задачи у больных сепсисом:
- восстановление адекватной тканевой перфузии,
- коррекция расстройств гомеостаза,
- нормализация клеточного метаболизма,
- снижение концентрации медиаторов септического каскада и токсических метаболитов.
При сепсисе с ПОН и септическом шоке стараются быстро (за первые 6 ч) достичь следующих значений важных показателей:
- гематокрит >30%,
- диурез 0,5 мл/(кгхч),
- сатурация крови в верхней полой вене или правом предсердии >70%,
- среднее АД >65 мм. рт. ст.,
- ЦВД 8-12 мм. рт. ст.
Поддержание перечисленных значений на указанном уровне повышает выживаемость пациентов (категория доказательств В). Мониторинг гемодинамики с помощью катетера Свана-Ганца (Swan-Ganz) и РIССО-технологии (транспульмональная термодилюция и анализ формы пульсовой волны) расширяют возможности контроля и оценки эффективности гемодинамической терапии, однако доказательств повышения выживаемости при их использовании не получено.
Величину оптимальной преднагрузки подбирают индивидуально, поскольку небходимо учитывать степень повреждения эндотелия и состояние лимфодренажа в лёгких, диастолическую функцию желудочков, а также изменения внутригрудного давления. Объем инфузионной терапии выбирают с таким расчетом, чтобы ДЗЛК не превышало КОД плазмы (профилактика ОЛ) и происходило повышение СВ. Дополнительно принимают во внимание параметры, характеризующие газообменную функцию легких (раО2 и раО2/FiO2) и изменения рентгенологической картины.
Для инфузионной терапии в рамках целенаправленного лечения сепсиса и септического шока практически с одинаковым результатом применяют кристаллоидные и коллоидные растворы.
Все инфузионные среды обладают как достоинствами, так и недостатками. На сегодняшний день, учитывая результаты экспериментальных и клинических исследований, нет оснований к предпочтению какого-либо определенного типа.
- Например, для адекватной коррекции венозного возврата и уровня преднагрузки необходимо ввести объем кристаллоидов в 2-4 раза больший, чем коллоидов, что связано с особенностями распределения растворов в организме Кроме того, инфузия кристаллоидов сопряжена с большим риском отека тканей, а их гемодинамический эффект короче, чем у коллоидов. В то же время кристаллоиды дешевле, не влияют на коагуляционный потенциал и не провоцируют анафилактоидных реакций. На основание вышеизложенного, качественный состав инфузионной программы определяют в зависимости от особенностей пациента учитывают степень гиповолемии, фазу синдрома ДВС, наличие периферических отеков и концентрацию альбумина в сыворотке крови, тяжесть острого легочного повреждения.
- Плазмозаменители (декстраны, препараты желатина, гидроксиэтилкрахмал) показаны при выраженном дефиците ОЦК. Гидроксиэтилкрахмалы со степенью замещения 200/0,5, 130/0,4 и 130/0,42 обладают потенциальным преимуществом перед декстранами в силу меньшего риска уклонения через мембрану и отсутствия клинически значимого воздействия на гемостаз.
- Введение альбумина при критических состояниях может увеличить риск летального исхода. Рост КОД при его инфузии носит транзиторный характер, а затем в условиях увеличения проницаемости капиллярного русла (синдром «капиллярной протечки») происходит дальнейшая экстравазация альбумина. Возможно, переливание альбумина будет полезным только при его концентрации в сыворотке менее 20 г/л и отсутствии признаков «утечки» в интерстиций.
- Применение криоплазмы показано при коагулопатии потребления и снижении коагуляционного потенциала крови.
- Широкое использование донорской эритроцитарной массы необходимо ограничивать ввиду высокого риска развития различных осложнений (ОПЛ, анафилактические реакции и т. д.). По мнению большинства специалистов, минимальная концентрация гемоглобина у больных с тяжелым сепсисом - 90-100 г/л.
Коррекция гипотензии
Низкое перфузионное давление требует немедленного включения препаратов, повышающих сосудистый тонус и/или инотропную функцию сердца. Допамин или норадреналин - средства первоочередного выбора для коррекции гипотензии у больных с септическим шоком.
Допамин (допмин) в дозе <10 мкг/(кгхмин) повышает АД, прежде всего за счёт увеличения СВ, и минимально действует на системное сосудистое сопротивление. В больших дозах преобладает его а-адренергический эффект, что приводит к артериальной вазоконстрикции, а в дозе <5 мкг/(кгхмин) допамин стимулирует дофаминергические рецепторы почечных, мезентериальных и коронарных сосудов, что приводит к вазодилатации, увеличению гломерулярной фильтрации и экскреции Nа+.
Норадреналин повышает среднее АД и увеличивает гломерулярную фильтрацию. Оптимизация системной гемодинамики под его действием ведет к улучшению функции почек без применения низких доз допамина Исследования последних лет показали, что его изолированное применение в сравнении с комбинацией с большими дозами допамина ведет к статистически значимому снижению летальности.
Адреналин - адренергический препарат с наиболее выраженными побочными гемодинамическими эффектами. Он обладает дозозависимым действием на ЧСС, среднее АД, СВ, работу левого желудочка, доставку и потребление О2. Однако одновременно возникают тахиаритмии, ухудшение органного кровотока, гиперлактатемия Поэтому применение адреналина ограничено случаями полной рефрактерности к другим катехоламинам.
Добутамин - препарат выбора для увеличения СВ и доставки и потребления О2 при нормальном или повышенном уровне преднагрузки. Благодаря преимущественному действию на бета1-адренорецепторы, он в большей степени, чем допамин, способствует повышению указанных показателей.
В экспериментальных исследованиях доказано, что катехоламины, помимо поддержки кровообращения, могут регулировать течение системного воспаления, влияя на синтез ключевых медиаторов, обладающих дистантным эффектом. Под действием адрналина, допамина, норадреналина и добутамина активированные макрофаги снижают синтез и секрецию ФНО-а.
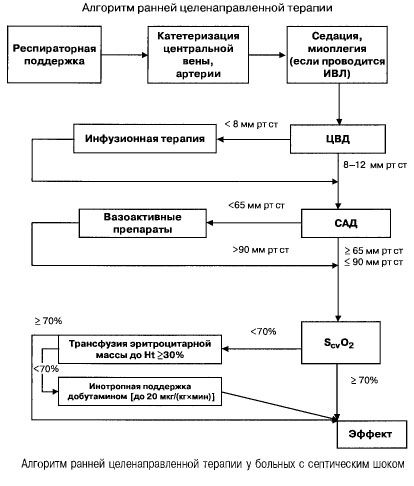
Выбор адренергических средств проводят по следующему алгоритму:
- сердечный индекс 3,5-4 л/(минхм2), SvО2 >70% - допамин или норадреналин,
- сердечный индекс <3,5 л/(минхм2), SvО2 <70% - добутамин (если систолическое АД <70 мм рт ст - вместе с норадреналином или допамином).
 [1],
[2],
[3],
[4],
[5],
[6],
[7],
[8]
[1],
[2],
[3],
[4],
[5],
[6],
[7],
[8]
Респираторная поддержка
Легкие - одни из первых органов-мишеней, вовлекаемых в патологический процесс при сепсисе. Острая дыхательная недостаточность - один из ведущих компонентов полиорганной дисфункции. Ее клинико-лабораторные проявления при сепсисе соответствуют ОПЛ, а при прогрессировании патологического процесса - ОРДС. Показания к проведению ИВЛ при тяжелом сепсисе определяют в зависимости от выраженности паренхиматозной дыхательной недостаточности (ОПЛ или ОРДС) Ее критерий - респираторный индекс:
- <200 - показана интубация трахеи и респираторная поддержка,
- >200 - показания определяют индивидуально.
Если при спонтанном дыхании с кислородной поддержкой больной в сознании, нет высоких затрат на работу дыхания и выраженной тахикардии (ЧСС <120 в минуту), нормальное значение венозного возврата S О2 >90%, то можно воздержаться от его перевода на ИВЛ. Однако необходимо внимательно следить за состоянием больного. Оптимальное значение S О2 - около 90%. Его можно поддерживать различными способами подачи газа (лицевые маски, носовые катетеры) в нетоксичных концентрациях (FiО2 <0,6). Неинвазивная ИВЛ противопоказана при сепсисе (категория доказательств В).
Следует избегать режимов высокообъёмной ИВЛ (ДО = 12 мл/кг), поскольку в подобных случаях возрастает секреция легкими цитокинов, что ведет к утяжелению ПОН. Необходимо придерживаться концепции безопасной ИВЛ, что возможно при соблюдении следующих условий (категория доказательств А):
- ДО <10 мл/кг,
- неинвертированное соотношение вдоха и выдоха,
- пиковое давление в дыхательных путях <35 см. вод. ст.,
- FiО2 <0,6.
Подбор параметров дыхательного цикла осуществляют до достижения адекватной ИВЛ, ее критерии раО2 >60 мм рт ст, SpО2 >88-93%, рvО2 35-45 мм рт ст, SvО2 >55%.
Один из эффективных методов оптимизации газообмена - проведение ИВЛ в положении на животе (Prone Positioning) (категория доказательств В). Подобная позиция эффективна у пациентов в наиболее тяжелом состоянии, хотя ее влияние на снижение летальности в отдаленном периоде статистически недостоверно.
Нутритивная поддержка
Проведение искусственной питательной поддержки - важный элемент лечения, одно из обязательных мероприятий, поскольку развитие синдрома ПОН при сепсисе, как правило, сопровождается проявлениями гиперметаболизма. В подобной ситуации покрытие энергетических потребностей происходит за счет деструкции собственных клеточных структур (аутоканнибализм), что усугубляет органную дисфункцию и усиливает эндотоксикоз.
Нутритивную поддержку рассматривают как метод профилактики тяжелого истощения (белково-энергетической недостаточности) на фоне выраженного усиления ката- и метаболизма. Включение энтерального питания в комплекс интенсивной терапии предупреждает перемещение кишечной микрофлоры, дисбактериоз, повышает функциональную активность энтероцитов и защитные свойства слизистой оболочки кишечника. Указанные факторы снижают степень эндотоксикоза и риск вторичных инфекционных осложнений.
Расчёт нутритивной поддержки:
- энергетическая ценность - 25-35 ккал/(кг массы тела х сут),
- количество белка - 1,3-2,0 г/(кг массы тела х сут),
- количество углеводов (глюкозы) - менее 6 г/кг/сут,
- количество жиров -0,5-1 г/кг/сут,
- дипептиды глутамина 0,3-0,4 г/кг/сут,
- витамины - стандартный суточный набор + витамин К (10 мг/сут) + витамины В1 и В6 (100 мг/сут) + витамины А, С, Е,
- микроэлементы - стандартный суточный набор + Zn (15-20 мг/сут + 10 мг/сут при наличии жидкого стула),
- электролиты - Na+, К+, Са2+ соответственно балансным расчетам и концентрации в плазме.
Раннее начало нутритивной поддержки (24-36 ч) более эффективно, чем на 3-4-е сут интенсивной терапии (категория доказательств В). Особенно - при энтеральном зондовом питании.
При тяжелом сепсисе преимуществ у энтерального или парентерального питания нет одинаковая длительность органных расстройств и сроки респираторной и инотропной поддержки, равные уровни летальности. Учитывая вышеизложенное, раннее энтеральное питание - более дешёвая альтернатива парентеральному Использование для зондового питания смесей, обогащенных пищевыми волокнами (пребиотиками) существенно снижает частоту диареи у больных с тяжёлым сепсисом.
Для эффективного синтеза белка в организме важно соблюдение метаболического соотношения «общий азот, г - небелковые калории, ккал» = 1-(110-130). Максимальная доза углеводов - 6 г/(кг массы телахсут), так как введение больших доз грозит гипергликемией и активацией катаболизма в скелетных мышцах. Жировые эмульсии рекомендуют вводить круглосуточно.
Противопоказания к нутритивной поддержке:
- декомпенсированный метаболический ацидоз,
- индивидуальная непереносимость сред нутритивной поддержки,
- резкая невосстановленная гиповолемия,
- рефрактерный шок - доза допамина >15 мкг/(кгхмин) и систолическое АД <90 мм рт ст,
- тяжёлая некупируемая артериальная гипоксемия.
Контроль гликемии
Важный аспект комплексного лечения тяжёлого сепсиса - постоянный контроль концентрации глюкозы в плазме крови и инсулинотерапия. Высокий уровень гликемии и необходимость его коррекции - факторы неблагоприятного исхода при сепсисе. Учитывая вышеизложенные обстоятельства, у больных поддерживают нормогликемию (4,5-6,1 ммоль/л), для чего при увеличении концентрации глюкозы выше допустимых значений проводят инфузию инсулина (0,5-1 ЕД/ч). В зависимости от клинической ситуации контроль концентрации глюкозы осуществляют через 1-4 ч. При выполнении указанного алгоритма отмечено статистически значимое повышение выживаемости больных.
Глюкокортикоиды
Результаты современных исследований в отношении эффективности использования глюкокортикоидов у больных с септическим шоком суммированы в следующих утверждениях:
- нецелесообразно использование гормонов в высоких дозах [метилпреднизолон 30-120 мг/(кгхсут) однократно или 9 сут, дексаметазон 2 мг/(кгхсут) 2 дня, бетаметазон 1 мг/(кгхсут) 3 дня] - увеличение риска госпитальных инфекций, отсутствие влияния на выживаемость,
- использование гидрокортизона в дозе 240-300 мг в сутки на протяжении 5-7 дней ускоряет стабилизацию гемодинамических показателей, позволяет отменить сосудистую поддержку и улучшает выживаемость у больных с сопутствующей относительной надпочечниковой недостаточностью (категория доказательств В).
Необходимо отказаться от хаотичного эмпирического назначения преднизолона и дексаметазона - нет оснований для экстраполяции на них новых сведений. В отсутствие лабораторных доказательств относительной надпочечниковой недостаточности гидрокортизон в дозе 300 мг в сутки (за 3-6 инъекций) вводят
- при рефрактерном шоке,
- если для поддержания эффективной гемодинамики необходимы высокие дозы вазопрессоров.
Возможно, в условиях системного воспаления при септическом шоке эффективность гидрокортизона связана с активацией ингибитора ядерного фактора kB (1кВ-а) и коррекцией относительной надпочечниковой недостаточности. В свою очередь, торможение активности транскрипционного ядерного фактора (NF-kB) ведет к снижению образования индуцибельной NO-синтетазы (NО - самый мощный эндогенный вазодилататор), провоспалительных цитокинов, ЦОГ и молекул адгезии.
Активированный протеин С
Одно из характерных проявлений сепсиса - нарушение системной коагуляции (активация коагуляционного каскада и угнетение фибринолиза), что в итоге приводит к гипоперфузии и органной дисфункции. Воздействие активированного протеина С на систему воспаления реализовано несколькими путями:
- снижение присоединения селектинов к лейкоцитам, что предохраняет от повреждения эндотелий, играющий важнейшую роль в развитии системного воспаления,
- снижение высвобождения цитокинов из моноцитов,
- блокирование высвобождения ФНО-а из лейкоцитов,
- угнетение выработки тромбина (он потенциирует воспалительный ответ).
Антикоагулянтное, профибринолитическое и противовоспалительное действие
- активированного протеина С обусловлено
- деградацией факторов Va и VIIIa - подавление тромбообразования,
- подавлением ингибитора активатора плазминогена - активация фибринолиза,
- прямым противовоспалительным эффектом на эндотелиальные клетки и нейтрофилы,
- защитой эндотелия от апоптоза
Введение активированного протеина С [дротрекогин альфа (активированный)] по 24 мкг/(кгхч) в течение 96 ч снижает риск летального исхода на 19,4%. Показания к назначению сепсис с острой ПОН и высоким риском смерти (APACHE II > 25 баллов, дисфункция 2 и более органов, категория доказательств В).
Активированный протеин С не снижает летальность у детей, пациентов с моноорганной дисфункцией, APACHE II < 25 баллов, у пациентов с нехирургическим сепсисом.
Иммуноглобулины
Целесообразность внутривенного введения иммуноглобулинов (IgG и IgG+IgM) связана с их способностью ограничивать избыточное действие провоспалительных цитокинов, повышать клиренс эндотоксинов и стафилококкового суперантигена, устранять анергию, усиливать эффект ß-лактамных антибиотиков Их использование в терапии тяжёлого сепсиса и септического шока - единственный метод иммунокоррекции, повышающий выживаемость. Наилучший эффект зарегистрирован при использовании комбинации IgG и IgM [RR=0,48 (0,35-0,75), категория доказательств А]. Стандартный режим дозирования - 3-5 мл/(кгхсут) 3 дня подряд. При использовании иммуноглобулинов наиболее оптимальные результаты получены в раннюю фазу шока («тёплый шок») и у пациентов с тяжелым сепсисом (состояние по шкале APACHE II - 20-25 баллов).
Профилактика тромбоза глубоких вен
Профилактика ТГВ нижних конечностей существенно влияет на результаты лечения больных с сепсисом (категория доказательств А). С указанной целью используют как нефракционированный, так и НМГ. Главные преимущества низкомолекулярных гепаринов - меньшая частота геморрагических осложнений, слабее выражено влияние на функцию тромбоцитов, продолжительное действие (возможность однократного введения в сутки).
Профилактика образования стресс-язв органов желудочно-кишечного тракта
Указанное направление играет существенную роль в благоприятном исходе при лечении больных с тяжелым сепсисом и септическим шоком, поскольку летальность при кровотечениях из стресс-язв органов ЖКТ составлает 64-87%. Без проведения профилактических мероприятий у больных в критическом состоянии стресс-язвы возникают в 52,8%. Однако использование ингибиторов протонного насоса и блокаторов Н2-рецепторов гистамина снижают риск более чем в 2 раза (первая группа препаратов эффективней второй). Основное направление профилактики и лечения - поддержание pH в пределах 3,5-6,0. Следует подчеркнуть, что помимо вышеуказанных препаратов важную роль в профилактике образования стресс-язв играет энтеральное питание.
Экстракорпоральное очищение крови
Различные биологически активные вещества и продукты метаболизма, участвующие в развитии генерализованного воспаления, - мишень для методов детоксикации, что особенно актуально при отсутствии естественного печёночно-почечного клиренса в условиях ПОН. Перспективными считают методы заместительной почечной терапии, способные воздействовать не только на уремические нарушения у больных с почечной недостаточностью, но и оказывать положительное влияние на другие изменения гомеостаза и органные дисфункции, возникающие при сепсисе, шоке и ПОН.
До настоящего времени нет данных, подтверждающих необходимость применения методов экстракорпорального очищения крови в качестве одного из основных направлений патогенетической терапии сепсиса и септического шока. Использование их оправдано при ПОН с доминированием почечной.
 [18],
[19],
[20],
[21],
[22],
[23]
[18],
[19],
[20],
[21],
[22],
[23]
Гемодиализ
Суть метода - диффузия веществ малой молекулярной массы (до 5х103 Да) через полупроницаемую мембрану и удаление избыточного количества жидкости из организма по градиенту давления. Гемодиализ широко применяют для лечения больных как с хронической, так и ОПН. Скорость диффузии веществ экспоненциально зависит от их молекулярной массы. Например, выведение олигопептидов происходит медленнее их синтеза.
Гемофильтрация
Гемофильтрация - эффективный способ удаления веществ с молекулярной массой 5х103- 5х104 Да и единственный способ выведения из организма большой группы биологически активных веществ и метаболитов Метод основан на конвекционном способе массопереноса. Помимо адекватной коррекции азотемии, в процессе гемофильтрации хорошо удаляются анафилатоксины СЗа, С5а, провоспалительные цитокины (ФНО-а, ИЛ-1b, 6 и 8), ß2-микроглобулин, миоглобин, паратгормон, лизоцим (молекулярная масса - 6000 Да), а-амилаза (молекулярная масса - 36 000-51 000 Да), креатинфосфокиназа, щелочная фосфатаза, трансаминазы и другие вещества. При гемофильтрации происходит удаление аминокислот и плазменных белков (в том числе иммуноглобулинов и циркулирующих иммунных комплексов).
Гемодиафильтрация
Гемодиафильтрация - наиболее мощный способ очищения крови, сочетает в себе диффузию и конвекцию (те ГД и ГФ). Дополнительный вклад в процесс детоксикации вносит сорбция патологических веществ на мембране фильтра.
Плазмаферез
Плазмаферез (плазмаобмен, плазмафильтрация) также рассматривают как возможный способ коррекции генерализованного воспаления у больных с сепсисом и септическим шоком Оптимальным считают применение плазмаобмена в постоянном режиме с удалением 3-5 объемов плазмы и одновременным её замещением на свежезамороженую, альбумин, коллоидные и кристаллоидные растворы. При коэффициенте просеивания 1 в процессе плазмафильтрации происходит хорошее удаление С-реактивного белка, гаптоглобина, СЗ фрагмента комплемента, 1-антитрипсина, ИЛ-6, тромбоксана-В2, гранулоцит-стимулирующего фактора, ФНО. Использование сорбентов для очистки плазмы самого пациента уменьшает риск заражения и снижает стоимость процедуры, поскольку исчезает необходимость применения чужеродных белков.
Применение длительной инфузии селенита натрия (селеназа) 1000 мкг/сут ири тяжёлом сепсисе приводит к снижению летальности.
Селен - незаменимый микроэлемент, значение которого связано с его ключевой ролью в антиоксидаитных системах клеток. Уровень селена в крови поддерживается в пределах 1,9-3,17 мкМ/л. Потребность в селене 50 -200 мкг в сут. причем она зависит от доступности других антиоксидантов и микроэлементов.
Селен мощный антиоксидант, компонент глютатионпероксидазы, фосфолинидглютатионпероксидазы, других оксиредуктаз и некоторых трансферам. Глютатионпероксидаза является важнейшим звеном эндогенной антиоксидант.
В течение последнего времени изучается эффективность селена при критических состояниях. Эти исследования показали, что основными механизмами действия селена являются:
- подавление гиперактивации NF-kB;
- уменьшение активации комплемента;
- действие его в качестве иммунномодулятора, антиоксиданта и противовоспалительного агента
- поддержание утилизации пероксидов;
- подавление эндотелиальной адгезии (снижение экспрессии ICAM-1, VCAM-2,
- Е - селектина, Р - селектина);
- защита эндотелия от кистородных радикалов (при помощи селенпротеина Р, предотвращающего образование пероксинитрита из О2, и NО).
Резюмируя вышеизложенное, можно определить конкретные задачи интенсивной терапии тяжелого сепсиса:
- Гемодинамическая поддержка ЦВД 8-12 мм рт ст, среднее АД >65 мм рт ст, диурез 0,5 мл/(кгхч), гематокрит >30%, сатурация смешанной венозной крови >70%.
- Респираторная поддержка пиковое давление в дыхательных путях <35 см вод ст, инспираторная фракция кислорода <60%, дыхательный объем <10 мл/кг, неинвертированное соотношение вдоха к выдоху.
- Глюкокортикоиды - «малые дозы» (гидрокортизон 240-300 мг в сутки).
- Активированный протеин С 24 мкг/(кгхч) в течение 4 сут при тяжелом сепсисе (APACHE II >25).
- Иммунокоррекция заместительная терапия пентаглобином.
- Профилактика тромбоза глубоких вен нижних конечностей.
- Профилактика образования стресс-язв органов желудочно-кишечного тракта применение ингибиторов протонного насоса и блокаторов Н2-рецепторов гистамина.
- Заместительная терапия ОПН.
- Нутритивная поддержка энергетическая ценность питания 25-30 ккал/кг массы тела х сут), белок 1,3-2,0 г/(кг массы тела х сут), дипептиды глутамина 0,3-0,4 г/(кг х сут), глюкоза - 30-70% от небелковых калорий, при условии поддержания гликемии <6,1 ммоль/л, жиры - 15-50% от небелковых калорий.

