Медицинский эксперт статьи
Новые публикации
Диагностика остеоартроза: магнитно-резонансная томография
Последняя редакция: 23.04.2024

Весь контент Web2Health проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
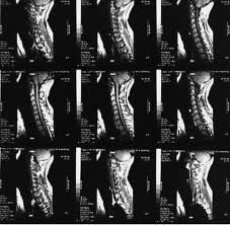
Магнитно-резонансная томография (МРТ) за последние годы стала одним из ведущих методов неинвазивной диагностики остеоартроза. С 70-х годов, когда принципы магнитного резонанса (MP) впервые стали использовать для исследования человеческого организма, до сегодняшних дней этот метод медицинской визуализации коренным образом изменился и продолжает быстро развиваться.
Совершенствуются техническое оснащение, программное обеспечение, развиваются методики получения изображений, разрабатываются MP-контрастные препараты. Это позволяет постоянно находить новые сферы применения МРТ. Если сначала ее применение ограничивалось лишь исследованиями центральной нервной системы, то сейчас МРТ с успехом применяют практически во всех областях медицины.
В 1946 г. группы исследователей из Стэндфордского и Гарвардского университетов независимо друг от друга открыли явление, которое было названо ядерно-магнитным резонансом (ЯМР). Суть его состояла в том, что ядра некоторых атомов, находясь в магнитном поле, под действием внешнего электромагнитного поля способны поглощать энергию, а затем испускать ее в виде радиосигнала. За это открытие Ф. Блоч и Е. Пармель в 1952 г. были удостоены Нобелевской премии. Новый феномен вскоре научились использовать для спектрального анализа биологических структур (ЯМР-спектроскопия). В 1973 г. Пауль Раутенбург впервые продемонстрировал возможность с помощью ЯМР-сигналов получить изображение. Так появилась ЯМР-томография. Первые ЯМР-томограммы внутренних органов живого человека были продемонстрированы в 1982 г. на Международном конгрессе радиологов в Париже.
Следует дать два пояснения. Несмотря на то, что метод основан на явлении ЯМР, его называют магнитно-резонансным (MP), опуская слово «ядерный». Это сделано для того, чтобы у пациентов не возникало мысли о радиоактивности, связанной с распадом ядер атомов. И второе обстоятельство: MP-томографы не случайно «настроены» именно на протоны, т.е. на ядра водорода. Этого элемента в тканях очень много, а ядра его обладают наибольшим магнитным моментом среди всех атомных ядер, что обусловливает достаточно высокий уровень МР-сигнала.
Если в 1983 г. во всем мире насчитывалось лишь несколько приборов, пригодных для клинических исследований, то к началу 1996 г. в мире работало около 10 000 томографов. Ежегодно в практику вводится 1000 новых приборов. Более 90% парка MP-томографов составляют модели со сверхпроводящими магнитами (0,5-1,5 Тл). Интересно отметить, что если в середине 80-х годов фирмы - производители MP-томографов руководствовались принципом «чем выше поле, тем лучше», делая упор на модели с полем 1,5 Тл и выше, то уже к концу 80-х годов стало ясно, что в большинстве областей применения они не имеют существенных преимуществ перед моделями со средней силой поля. Поэтому основные производители MP-томографов («Дженерал Электрик», «Сименс», «Филипс», «Тоши-ба», «Пикер», «Брукер» и др.) в настоящее время большое внимание уделяют выпуску моделей со средним и даже низким полем, которые отличаются от высокопольных систем компактностью и экономичностью при удовлетворительном качестве изображений и значительно меньшей стоимости. Высокопольные системы используются преимущественно в научно-исследовательских центрах для проведения МР-спектроскопии.
Принцип метода МРТ
Основными компонентами MP-томографа являются: сверхсильный магнит, радиопередатчик, приемная радиочастотная катушка, компьютер и пульт управления. Большинство аппаратов имеют магнитное поле с магнитным моментом, параллельным длинной оси тела человека. Сила магнитного поля измеряется в теслах (Тл). Для клинической МРТ используют поля с силой 0,2-1,5 Тл.
Когда пациента помещают в сильное магнитное поле, все протоны, являющиеся магнитными диполями, разворачиваются в направлении внешнего поля (подобно компасной стрелке, ориентирующейся на магнитное поле Земли). Помимо этого, магнитные оси каждого протона начинают вращаться вокруг направления внешнего магнитного поля. Это специфическое вращательное движение называют процессией, а его частоту - резонансной частотой. При пропускании через тело пациента коротких электромагнитных радиочастотных импульсов магнитное поле радиоволн заставляет магнитные моменты всех протонов вращаться вокруг магнитного момента внешнего поля. Для того чтобы это произошло, необходимо, чтобы частота радиоволн была равна резонансной частоте протонов. Это явление называют магнитным резонансом. Для изменения ориентации магнитных протонов магнитные поля протонов и радиоволн должны резонировать, т.е. иметь одинаковую частоту.
В тканях пациента создается суммарный магнитный момент: ткани намагничиваются и их магнетизм ориентируется строго параллельно внешнему магнитному полю. Магнетизм пропорционален числу протонов в единице объема ткани. Огромное число протонов (ядер водорода), содержащихся в большинстве тканей, обусловливает тот факт, что чистый магнитный момент достаточно велик для того, чтобы индуцировать электрический ток в расположенной вне пациента принимающей катушке. Эти индуцированные MP-сигналы используются для реконструкции МР-изображения.
Процесс перехода электронов ядра из возбужденного состояния в равновесное называется спин-решеточным релаксационным процессом или продольной релаксацией. Он характеризуется Т1 - спин-решеточным временем релаксации - временем, необходимым для перевода 63% ядер в состояние равновесия после их возбуждения 90° импульсом. Выделяют также Т2 - спин-спиновое время релаксации.
Существует ряд способов получения MP-томограмм. Их различие заключается в порядке и характере генерации радиочастотных импульсов, методах анализа MP-сигналов. Наибольшее распространение имеют два способа: спин-решеточный и спин-эховый. При спин-решеточном анализируют главным образом время релаксации Т1. Различные ткани (серое и белое вещество головного мозга, спинномозговая жидкость, опухолевая ткань, хрящ, мышцы и т.д.) имеют в своем составе протоны с разным временем релаксации Т1. С продолжительностью Т1 связана интенсивность MP-сигнала: чем короче Т1, тем интенсивнее МР-сигнал и тем светлее выглядит данное место изображения на телемониторе. Жировая ткань на MP-томограммах - белая, вслед за ней по интенсивности MP-сигнала в порядке убывания идут головной и спинной мозг, плотные внутренние органы, сосудистые стенки и мышцы. Воздух, кости и кальцификаты практически не дают MP-сигнала и поэтому отображаются черным цветом. Указанные взаимоотношения времени релаксации Т1 создают предпосылки для визуализации нормальных и измененных тканей на МР-томограммах.
При другом способе MP-томографии, названном спин-эховым, на пациента направляют серию радиочастотных импульсов, поворачивающих прецессирующие протоны на 90°. Вслед за прекращением подачи импульсов регистрируют ответные MP-сигналы. Однако интенсивность ответного сигнала по-иному связана с продолжительностью Т2: чем короче Т2, тем слабее сигнал и, следовательно, ниже яркость свечения экрана телемонитора. Таким образом, итоговая картина МРТ по способу Т2 противоположна таковой по способу Т1 (как негатив позитиву).
На MP-томограммах лучше, чем на компьютерных томограммах, отображаются мягкие ткани: мышцы, жировые прослойки, хрящи, сосуды. На некоторых аппаратах можно получить изображение сосудов, не вводя в них контрастное средство (MP-ангиография). Вследствие невысокого содержания воды в костной ткани последняя не создает экранирующего эффекта, как при рентгеновской компьютерной томографии, т.е. не мешает изображению, например, спинного мозга, межпозвоночных дисков и т.д. Конечно, ядра водорода содержатся не только в воде, но в костной ткани они фиксированы в очень больших молекулах и плотных структурах и не являются помехой при МРТ.
Преимущества и недостатки метода МРТ
К основным достоинствам МРТ относятся неинвазивность, безвредность (отсутствие лучевой нагрузки), трехмерный характер получения изображений, естественный контраст от движущейся крови, отсутствие артефактов от костных тканей, высокая дифференциация мягких тканей, возможность выполнения MP-спектроскопии для прижизненного изучения метаболизма тканей in vivo. MPT позволяет получать изображение тонких слоев тела человека в любом сечении - во фронтальной, сагиттальной, аксиальной и косых плоскостях. Можно реконструировать объемные изображения органов, синхронизировать получение томограмм с зубцами электрокардиограммы.
К основным недостаткам обычно относят достаточно большое время, необходимое для получения изображений (обычно минуты), что приводит к появлению артефактов от дыхательных движений (это особенно снижает эффективность исследования легких), аритмий (при исследовании сердца), невозможность надежного выявления камней, кальцификатов, некоторых видов патологии костных структур, высокая стоимость оборудования и его эксплуатации, специальные требования к омещениям, в которых находятся приборы (экранирование от помех), невозможность обследования больных с клаустрофобией, искусственными водителями ритма, крупными металлическими имплантатами из немедицинских металлов.
 [8],
[9],
[10],
[11],
[12],
[13],
[14],
[15]
[8],
[9],
[10],
[11],
[12],
[13],
[14],
[15]
Контрастные вещества для МРТ
В начале использования МРТ считалось, что естественная контрастность между различными тканями исключает необходимость применения контрастных веществ. Вскоре было обнаружено, что разница в сигналах между различными тканями, т.е. контрастность МР-изображения может быть существенно улучшена контрастными средствами. Когда первое MP-контрастное средство (содержащее парамагнитные ионы гадолиния) стало коммерчески доступным, диагностическая информативность МРТ значительно возросла. Суть применения МР-контрастного средства состоит в том, чтобы изменить магнитные параметры протонов тканей и органов, т.е. изменить время релаксации (TR) Т1 и Т2 протонов. На сегодняшний день существует несколько классификаций MP-контрастных средств (или вернее контрастных агентов - КА).
По преимущественному влиянию на время релаксации МР-КАделят на:
- Т1-КА, которые укорачивают Т1 и тем самым повышают интенсивность MP-сигнала тканей. Их еще называют позитивными КА.
- Т2-КА, которые укорачивают Т2, снижая интенсивность МР-сигнала. Это негативные КА.
В зависимости от магнитных свойств МР-КА подразделяются на парамагнитные и суперпарамагнитные:
Парамагнитные контрастные средства
Парамагнитными свойствами обладают атомы с одним или несколькими неспаренными электронами. Это магнитные ионы гадолиния (Gd), хрома, никеля, железа, а также марганца. Наиболее широкое клиническое применение получили соединения гадолиния. Контрастирующий эффект гадолиния обусловлен укорочением времени релаксации Т1 и Т2. В низкихдозах преобладает воздействие на Т1, повышающее интенсивность сигнала. В высоких дозах преобладает воздействие на Т2 со снижением интенсивности сигнала. Парамагнетики сейчас наиболее широко используются в клинико-диагностической практике.
Суперпарамагнитные контрастные средства
Доминирующим воздействием суперпарамагнитного оксида железа является укорочение релаксации Т2. С повышением дозы происходит снижение интенсивности сигнала. К этой группе КА можно отнести и ферромагнитные КА, в состав которых входят ферромагнитные оксиды железа, структурно сходные с ферритом магнетита (Fe2+OFe23+03).
Следующая классификация основана на фармакокинетике КА (СергеевП.В. исоавт., 1995):
- внеклеточные (тканенеспецифические);
- желудочно-кишечные;
- органотропные (тканеспецифические);
- макромолекулярные, которые используют для определения сосудистого пространства.
В Украине известны четыре МР-КА, которые являются внеклеточными водорастворимыми парамагнитными КА, из них широко используют гадодиамид и гадопентетовую кислоту. Остальные группы КА (2-4) проходят стадию клинических испытаний за рубежом.
Внеклеточные водорастворимые МР-КА
|
Международное название |
Химическая формула |
Структура |
|
Гадопентетовая кислота |
Гадолиния димеглюмина диэтилентриаминпента-ацетат ((NMG)2Gd-DTPA) |
Линейная, ионная |
|
Кислота гадотеровая |
(NMG)Gd-DOTA |
Циклическая, ионная |
|
Гадодиамид |
Гадолиния диэтилентриаминпентаацетат-бис-метиламид (Gd-DTPA-BMA) |
Линейная, неионная |
|
Гадотеридол |
Gd-HP-D03A |
Циклическая, неионная |
Внеклеточные КА вводят внутривенно, на 98% они выделяются почками, не проникают через гематоэнцефалический барьер, обладают низкой токсичностью, относятся к группе парамагнетиков.
Противопоказания к проведению МРТ
К абсолютным противопоказаниям относят состояния, при которых проведение исследования является угрожающим жизни пациентов. Например, наличие имплантатов, которые активируются электронным, магнитным или механическими путями, - это в первую очередь искусственные водители ритма. Воздействие радиочастотного излучения МР-томографа может нарушить функционирование стимулятора, работающего в системе запроса, так как изменения магнитных полей могут имитировать сердечную деятельность. Магнитное притяжение может вызвать также смещение стимулятора в гнезде и сдвинуть электроды. Кроме того, магнитное поле создает препятствия для работы ферромагнитных или электронных имплантатов среднего уха. Наличие искусственных клапанов сердца представляет опасность и является абсолютным противопоказанием только при исследовании на МР-томографах с высокими полями, а также если клинически предполагается повреждение клапана. К абсолютным противопоказаниям к исследованию относится также наличие небольших металлических хирургических имплантатов (гемостатические клипсы) в центральной нервной системе, так как смещение их вследствие магнитного притяжения угрожает кровотечением. Их наличие в других частях тела имеет меньшую угрозу, так как после лечения фиброз и инкапсулирование зажимов помогают удержать их в стабильном состоянии. Однако помимо потенциальной опасности, наличие металлических имплантатов с магнитными свойствами в любом случае вызывает артефакты, создающие сложности для интерпретации результатов исследования.
Противопоказания к проведению МРТ
|
Абсолютные: |
Относительные: |
|
Кардиостимуляторы |
Прочие стимуляторы (инсулиновые насосы, нервные стимуляторы) |
|
Ферромагнитные или электронные имплантаты среднего уха |
Неферромагнитные имплантаты внутреннего уха, протезы клапанов сердца (в высоких полях, при подозрении на дисфункцию) |
|
Кровоостанавливающие клипсы сосудов головного мозга |
Кровоостанавливающие клипсы прочей локализации, декомпенсированная сердечная недостаточность, беременность, клаустрофобия, необходимость в физиологическом мониторинге |
К относительным гротивопоказаниям, помимо перечисленных выше, относятся также декомпенсированная сердечная недостаточность, необходимость физиологического мониторинга (механическая вентиляция легких, электрические инфузионные насосы). Клаустрофобия является препятствием для проведения исследования в 1-4% случаев. Преодолеть его можно, с одной стороны, использованием приборов с открытыми магнитами, с другой - подробным объяснением устройства аппаратуры и хода обследования. Свидетельств повреждающего действия МРТ на эмбрион или плод не получено, однако рекомендовано избегать МРТ в I триместре беременности. Применение МРТ в период беременности показано в случаях, когда другие неионизирующие методы диагностической визуализации не дают удовлетворительной информации. МРТ-исследование требует большего участия в нем пациента, чем компьютерная томография, так как движения больного во время исследования значительно сильнее влияют на качество изображений, поэтому исследование больных с острой патологией, нарушенным сознанием, спастическими состояниями, деменцией, а также детей нередко бывает затруднительным.

