Жидкостная цитология шейки матки
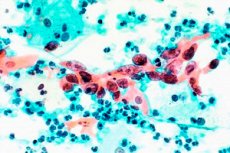
Жидкостная цитология шейки матки – это инновационный метод цитологического исследования, «золотой стандарт» диагностирования неоплазий слизистой оболочки канала и влагалищной части маточной шейки, который применяется при подозрении у пациентки на рак или дисплазию. Благодаря такому способу диагностики можно обнаружить рак на самых ранних стадиях развития, что увеличивает шансы на полное излечение.
После забора мазка на онкоцитологию биологический материал помещается в определенную жидкую среду. С помощью специальной центрифуги происходит «отмывание» клеток (цито-препаратов), которые концентрируются в одном месте и образуют ровный слой. В данном случае заключение врача-цитолога будет более точным и информативным, нежели при обычной цитологии, когда материал, взятый для исследования, сразу же наносится на медицинское стекло для анализов.
Сегодня в медицине все чаще применяется технология ПАП-теста (ThinPrep). Преимуществом этой инновации является высокая четкость изображения клеток. При использовании данной технологии полученный материал смешивается со специальным раствором, который механически отделяет клетки эпителия от загрязнений. В результате такого исследования число ложно-отрицательных ответов намного сокращается.
Показания
Жидкостная цитология шейки матки как гинекологический метод исследования помогает в выборе наиболее эффективных способов лечения онкозаболевания. С помощью данного метода можно определить наличие злокачественных клеток, а также степень развития болезни. Цервикальный скрининг целесообразно проводить с началом половой жизни. В группу риска можно отнести женщин с вирусом папилломы.
Показания для проведения исследования:
- планирование беременности;
- нарушение или сбои менструального цикла (слишком короткий или удлиненный цикл, частые задержки);
- бесплодие;
- наличие нескольких сексуальных партнеров;
- гинекологические патологии вирусной этиологии (остроконечные кондиломы, генитальный герпес и пр.);
- длительный прием противозачаточных и гормональных препаратов;
- беспричинное появление влагалищных выделений;
- подготовка к установке контрацептивных средств (внутриматочной спирали и т.п.).
Цервикальный скрининг направлен на диагностику папилломавирусной инфекции и поражений шейки матки и принятие лечебно-профилактических мер. Мазок рекомендуется сдавать в первую неделю после окончания менструации. Результат может быть «нормальным» (отрицательным), указывающим на отсутствие патологий в шейке матки, и «патологическим» (положительным), – если в образце выявлены атипичные клетки, которые впоследствии могут привести к развитию рака.
Преимущества жидкостной цитологии
Жидкостная цитология шейки матки позволяет получить наиболее точный результат исследования клеток на наличие либо отсутствие патологий.
Преимущества жидкостной цитологии – в улучшенном качестве полученного биоматериала. Кроме того, нужно отметить:
- быстрое приготовление препарата;
- продолжительный срок годности и хранения материала (с помощью стабилизирующего раствора PreservCyt удается предотвратить высыхание клеток; это позволяет сохранять образец в наиболее благоприятных условиях для его последующей транспортировки в медицинскую лабораторию);
- возможность приготовления нескольких цитологических препаратов из полученного биоматериала;
- применение стандартизированных методик окрашивания;
- возможность приготовления монослойного мазка.
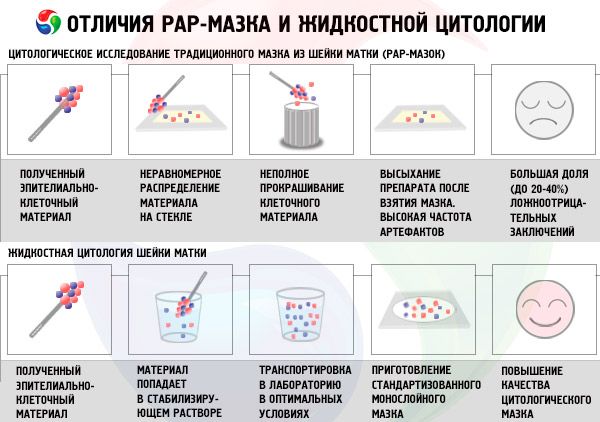
Применение жидкостной цитологии – новой технологии обследования на рак, по сравнению с традиционным методом, позволяет существенно повысить качество цитологического мазка, а также предоставляет возможность использовать дополнительные методы диагностики без вторичного гинекологического обследования.
Скрининговый метод рекомендуется применять с определенной регулярностью для своевременного предупреждения онкологических заболеваний шейки матки. Он позволяет выявить начальные стадии рака, а также предраковые и фоновые процессы цервикального эпителия.
Подготовка
Жидкостная цитология шейки матки – это быстрый и доступный метод гинекологического исследования, с помощью которого можно получить точную информацию о каких-либо отклонениях в клетках шейки матки. Забор мазка осуществляется в период осмотра пациентки в гинекологическом кресле.
Подготовка к данной процедуре включает воздержание от:
- сексуальных отношений за 2-е суток до взятия мазка;
- спринцеваний (санаций) влагалища;
- применения вагинальных свечей и спермицидных мазей;
- приема контрацептивных и противовоспалительных средств (таблеток);
- введения тампонов во влагалище.
Необходимо подчеркнуть, что анализ на жидкостную цитологию является одним из самых информативных. Забор мазка происходит быстро и безболезненно, – данный метод обследования широко используется в гинекологии. За 2-3 ч. до проведения ПАП-теста нужно воздержаться от мочеиспускания. Нельзя делать анализ в дни менструации, при влагалищных выделениях, зуде, наличии воспалительного процесса.
Сама процедура очень проста: врач-гинеколог очищает шейку матки ватным тампоном, а затем с помощью специальной щеточки осуществляет забор материала для анализа и наносит его на медицинское стекло. После этого проводится лабораторное исследование содержимого под микроскопом. О результатах анализа можно будет узнать примерно через 7-10 дней. Цитологический мазок позволяет определить форму, размеры, порядок размещения клеток, что помогает диагностировать болезни шейки матки, в том числе раковые и предраковые состояния. Данное обследование рекомендуется проводить не реже 1 раза в год.
Оборудование для жидкостной цитологии
Жидкостная цитология шейки матки является инновационным методом обследования, который позволяет осуществить точную диагностику влагалищного мазка с целью выявления онкозаболевания. Тест ПАП был введен в медицину греческим ученым Джорджем Папаниколау и за короткий промежуток времени помог существенно снизить уровень смертности пациенток с диагнозом «рак шейки матки», а также другими патологиями (эндометрием и пр.). С помощью данного метода удается получить прогноз с более высокой степенью вероятности, нежели при простом цитологическом анализе.
В процессе забора мазка на онкоцитологию врач-гинеколог использует цитощетку особой формы, которая вместе с биоматериалом помещается в специальный стабилизирующий раствор. Клетки, таким образом, удается полностью сохранить, что гарантирует более качественный, точный и достоверный результат.
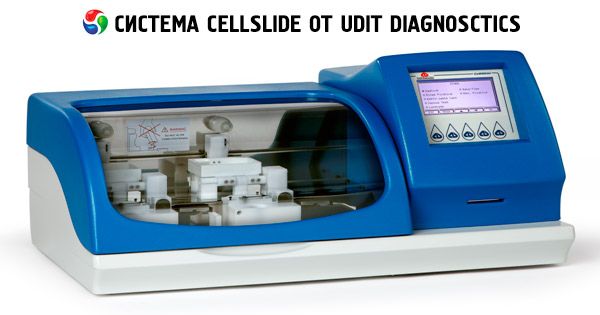
Оборудование для жидкостной цитологии – это автоматический процессор, выполняющий операции по изготовлению цитопрепарата с помощью четко заданной программы. Повышению качества исследования способствует равномерное распределение цитопрепарата на специальном слайде-стекле.
Для анализа применяется определенный объем биоматериала, после чего клетки проходят через вакуумный фильтр, очищаясь от таких загрязнений, как слизь и кровь. Для проведения дальнейшей микроскопии на предметное стекло помещается однородный слой клеток. Размещенный на стекле-слайде очищенный препарат обеспечивает более высокую точность как самого процесса исследования, так и полученного результата.
Следует подчеркнуть, что при использовании метода жидкостной цитологии чувствительность теста достигает 95 %, в то время как при традиционном цитологическом анализе – лишь 40-60 %. По рекомендации ВОЗ жидкостная цитология является «золотым стандартом» исследования мазка. Высокая точность результата достигается путем использования комбинированной цитощетки, стабилизирующего раствора и фильтрации. Это позволяет своевременно диагностировать рак шейки матки и принять необходимые меры для эффективного лечения.
Техника проведения
Жидкостная цитология шейки матки основана на лабораторном исследовании отобранного биоматериала. Поскольку рак шейки развивается на протяжении длительного периода времени (несколько лет), регулярное обследование поможет выявить патологию на ранних стадиях развития онкозаболевания. Таким образом, лечение будет более эффективным.
Техника проведения жидкостной цитологии довольно проста: обследование проводится с применением гинекологического кресла. Перед началом процедуры во влагалище вводится гинекологическое зеркало с целью визуального осмотра его канала и шейки. Затем шейка очищается от выделений ватным тампоном. С помощью стерильной цервикальной щеточки (эндобраша) врач-гинеколог осуществляет забор биоматериала (соскоб). Образец помещается в специальный раствор, предотвращающий высыхание клеток, а затем распределяется по стеклу. Такой раствор очищает биоматериалы от загрязнений (слизи и лейкоцитов) и сохраняет целостность клеток эпителия. Процедура абсолютно безболезненна и занимает немного времени. Результаты анализа будут готовы примерно через неделю.
Достоверные результаты можно получить только при четком соблюдении техники взятия мазка. Анализ необходимо проводить не ранее чем на пятый день после начала менструального цикла и не позднее 5-го дня до предполагаемого начала менструации. Результат будет недостоверным, если перед забором материала во влагалище вводились какие-либо медицинские препараты (свечи, контрацептивные средства), осуществлялись санации влагалища, а также за 24 часа до проведения жидкостной цитологии имел место половой акт.
Жидкостная PAP-цитология
Жидкостная цитология шейки матки является наиболее информативным методом гинекологического исследования на наличие атипичных (раковых) клеток. На сегодняшний день это регулярный тест, который проводится при обычном гинекологическом осмотре женщин.
Жидкостная пап цитология (Пап-тест) представляет собой исследование мазков (клеточных образцов), взятых с поверхности шейки. Этот метод был открыт в 20-х гг. прошлого века Джорджем Папаниколау – греческим ученым и медиком, который, проводя исследования на крысах и делая им мазки с ЦК, обнаруживал инфекции и опухоли. Таким образом, ученому пришла в голову мысль использовать данный метод цитологической диагностики при обследовании женщин. Официально он стал применяться в 1943 году.
Тест направлен на своевременное выявление и диагностирование рака шейки матки. Он основан на применении способа окрашивания взятых образцов аналогично микроскопическому исследованию. С помощью окраски удается определить реакцию клеточных структур на основные и кислые красители. Сегодня он практикуется во всем мире как один из основных способов исследования онкологических заболеваний.
Забор мазка осуществляется с помощью шпателя Эйра (специальной щеточки). Образцы переносятся на стекло, а затем обрабатываются фиксирующим раствором и отправляются в медицинскую лабораторию для тщательного исследования с использованием окраски. Это помогает определить реактивный, воспалительный, доброкачественный или злокачественный процессы. В большинстве случаев при помощи Пап-теста удается идентифицировать малейшую патологию шейки матки на клеточном уровне еще до развития онкозаболевания, что позволяет вовремя назначить эффективное лечение.
Мазок на жидкостную цитологию
Жидкостная цитология шейки матки – простой и точный анализ, с помощью которого можно оценить состояние тканей и выявить возможные патологии. Процедура вполне безопасна и относительно безболезненна. Главная цель данного исследования – выявление атипичных клеток, которые со временем могут переродиться в раковую опухоль. Своевременная диагностика неблагоприятных изменений и патологий на самых ранних стадиях сделает лечение более быстрым и эффективным.
Мазок на жидкостную цитологию помогает определить общее состояние слизистой оболочки и выявить патологию. На сегодняшний день именно этот метод гинекологического исследования считается наиболее доступным и достоверным. С помощью мазка можно определить состав микрофлоры влагалища, а также степень ее чистоты. Для получения максимально точного результата о состоянии шейки матки врач-гинеколог может провести ряд дополнительных анализов (кольпоскопию, биопсию).
Данное исследование помогает выявить вирусные инфекции и другие факторы, которые могут спровоцировать развитие опухоли. Мазок берется специальной щеточкой из трех разных зон слизистой влагалища: из самого канала шейки, его поверхности и сводов. Образцы погружаются во флакон с раствором, предотвращающим высыхание клеток и их бактериальное «засорение», а затем наносятся на специальное стекло и отправляются в медицинскую лабораторию для тщательного изучения. С этой целью используется способ окрашивания по Папаниколау.
Раствор, используемый при цитологическом исследовании, устойчив к резким колебаниям температуры, а также гарантирует многолетнее хранение клеточного материала, что дает возможность проводить дополнительные анализы на весь спектр генитальных инфекций, включая генетическое тестирование на ВПЧ. Таким образом, для проведения всех исследований можно использовать один и тот же флакон с жидкостным цитологическим материалом. При этом дополнительных визитов к врачу от пациентки не потребуется.
Расшифровка результатов
Жидкостная цитология шейки матки – самый простой и достоверный метод гинекологического обследования, позволяющий выявить различные патологии, в том числе рак на ранних стадиях развития.
Расшифровка результатов данного цитологического исследования направлена на оценку состояния клеток эпителия. Всего выделяют 5 состояний (стадий развития, классов) заболевания:
- 1 – в строении клеток нет патологических нарушений, норма;
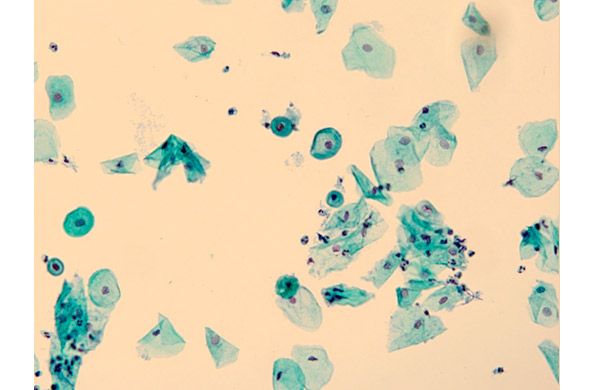
- 2 – наблюдается снижение морфологической нормы некоторых элементов клетки; подозрение на воспаление или заболевание инфекционного характера (например, вагиноз); для более точного диагноза и назначения лечения понадобятся дополнительные методы обследования – кольпоскопия и/или биопсия;
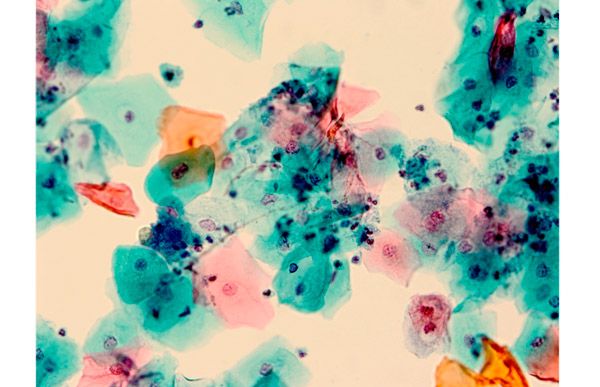
- 3 – аномальные изменения наблюдаются в единичных клетках; необходимо повторное исследование;
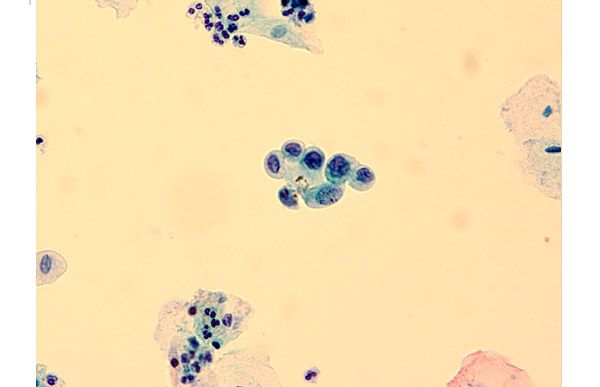
- 4 – злокачественные изменения в строении клеток, которые указывают на предраковое состояние;
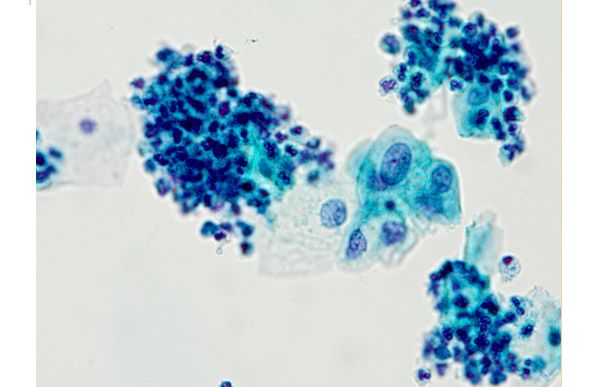
- 5 – обнаружено большое количество атипичных клеток, что указывает на начальную степень развития раковой опухоли.
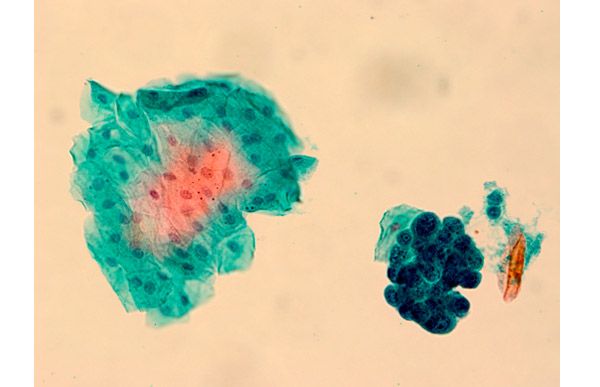
Для получения максимально точных результатов расшифровка анализов происходит по системе Бетесда. Конечный диагноз устанавливается на основании полученной информации об изменениях в клеточном ядре и расположении клеток. ЦБО – аббревиатура, указывающая на норму всех показателей.
Следующие аббревиатуры используются в расшифровке результатов анализа для обозначения различных патологических изменений:
- ASC-US – наблюдаются изменения плоских клеток эпителия; часто такой показатель встречается у женщин в возрасте от 45-ти лет в связи со снижением уровня эстрогена;
- AGC – выявлены измененные цилиндрические клетки, что является показателем воспалительных заболеваний (например, вагиноза);
- LSIL – имеется небольшой процент атипичных клеток не раковой этиологии;
- ASC-H – обнаружены нарушения в клеточном строении, что указывает на предраковое состояние (дисплазию) или начальную стадию развития рака;
- HSIL – данная аббревиатура указывает на онкоцитологию, что подтверждается наличием в образце измененных плоских клеток;
- AIS – наличие в мазке клеток цилиндрического эпителия, что указывает на рак.
Осложнения
Жидкостная цитология шейки матки – процедура безболезненная и несложная. В то же время она дает наиболее информативный результат о наличии или отсутствии каких-либо патологий. Это эффективный метод диагностики рака шейки матки на первых стадиях развития заболевания. Забор мазка на онкоцитологию должен осуществлять врач-специалист, владеющий техникой данного процесса.
Осложнения после проведения обследования обычно не возникают. В некоторых случаях могут отмечаться лишь небольшие кровянистые выделения из влагалища, которые проходят через 2-3 дня и не требуют специального лечения. После манипуляций может также возникнуть выраженная болезненность. Такие симптомы считаются нормой, однако если к ним присоединились другие признаки (повышение температуры, озноб, сильные боли), необходимо обратиться к врачу.
При неправильном заборе мазка могут возникнуть опасные последствия. Так, грубое вмешательство провоцирует развитие стеноза в результате образования спаек. Поэтому не принято осуществлять взятие мазка на цитологию в глубоких зонах цервикального канала. Во избежание каких-либо осложнений женщине рекомендуется в течение 7-10 дней после проведения ПАП-теста отказаться от сексуальных отношений, использования тампонов и влагалищного спринцевания.
Выделения после жидкостной цитологии
Жидкостная цитология шейки матки – эффективный метод, применяющийся в гинекологии для выявления патологий, связанных с воспалительными или инфекционными заболеваниями, а также развитием рака. Обычно процедура безболезненная и не доставляет женщине каких-либо неудобств.
Выделения после жидкостной цитологии могут наблюдаться приблизительно 5-7 дней после проведения исследования. Чаще всего они имеют темно-коричневый или грязно-зеленый оттенок. Это нормальное явление, поэтому специального лечения не потребуется. В этот период рекомендуется использовать обычные гигиенические прокладки.
Если женщина жалуется на обильные кровянистые выделения и выраженную болезненность после взятия мазка, – вероятнее всего, техника забора цитологического материала была нарушена. В таком случае необходимо обратиться к врачу для предотвращения возможных осложнений, из которых можно отметить стеноз канала, спровоцированный спайками. Такое осложнение возможно при грубом вмешательстве в зону цервикального канала.
В течение нескольких дней после проведения данного исследования необходимо понаблюдать за состоянием. Если кровянистые выделения сопровождаются повышением температуры, ознобом, болями в животе, следует как можно скорее обратиться за медицинской помощью.
Жидкостная цитология шейки матки относится к «золотому стандарту» исследований, направленных на своевременное диагностирование онкозаболевания. С помощью данного гинекологического метода можно выявить предраковые состояния, а также злокачественные изменения на ранних стадиях. Помимо клеточных аномалий, цервикальный мазок дает возможность «определить» наличие патогенных микроорганизмов, половых инфекций, вирусов и оценить состояние слизистой. Каждой женщине нужно помнить о важности и необходимости регулярного (ежегодного) обследования.
Медицинский рецензент, редактор
Портнов Алексей Александрович
Образование: Киевский Национальный Медицинский Университет им. А.А. Богомольца, специальность - "Лечебное дело"
