Медицинский эксперт статьи
Новые публикации
Диагностика рака молочной железы
Последняя редакция: 06.07.2025

Весь контент Web2Health проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
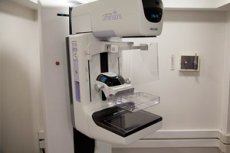
Диагностика рака молочной железы – это комплекс методов, направленных на выявление злокачественных опухолей. От раннего выявления этой патологии зависит эффективность лечения и прогноз выздоровления. Рассмотрим основные процедуры, используемые для выявления злокачественных поражений.
Рак молочной железы – это самая распространенная форма опухоли у женщин, она занимает 19% среди всех злокачественных новообразований. Риск злокачественных новообразований увеличивается прямо пропорционально возрасту. Самый большой процент смертельного исхода приходится на женщин 40-55 лет. У мужчин, рак груди диагностируют очень редко. Существует ряд факторов риска, которые могут стать причиной злокачественного новообразования. Основные факторы: период менопаузы, фиброзно-кистозная мастопатия, отсутствие родов или роды после 30 лет, семейный анамнез и другое.
Локализация опухоли в молочной железе бывает разная. С одинаковой частотой встречается поражение как левой, так и правой железы, а в 25% случаев наблюдается двустороннее раковое поражение. При этом узел во второй железе может быть как самостоятельной опухолью, так и метастазом. Чаще всего опухоли появляются в верхнее-наружном квадрате или возле подмышечной впадины. Основная симптоматика заболевания, проявляется как уплотнение и втяжение соска, кровянистые выделения из груди, болевые ощущения.
Кроме классической клинической картины, в процессе диагностирования могут быть выявлены такие формы заболевания:
- Маститоподобный
Резким увеличение молочной железы, отек, болезненностью. Кожа становится горячей на ощупь, приобретает красный цвет. Для выявления матистоподобного рака проводят дифференциальный диагноз с острым маститом.
- Рожистоподобная форма
При внешнем осмотре первое, на что обращают внимание – это красная кожа, при этом краснота распространяется и за пределы груди. Помимо покраснения кожи, у больной наблюдается высокий подъем температуры. Диагностирование должна проводиться опытным врачом, так как зачастую данную форму злокачественного новообразования путают с обычным рожистым воспалением.
- Панцирный
Появляется из-за раковой инфильтрации по щелям кожи и лимфатическим сосудам. Кожа утолщается и приобретает бугристость. На груди образуется толстый кожный панцирь, который может охватывать как одну, так и обе железы. Заболевание имеет высшую степень злокачественности.
- Рак Пэджета
Является плоскостным поражением сосков и ареолов. При ранней диагностике, основной признак поражения – мокнущие и шелушащие соски, которые ошибочно могут принимать за экзему. При дальнейшем развитии, рак прорастает в протоки железы и формирует узел с метастатическими поражениями лимфатических узлов.
Задача врача выявить всю типичную симптоматику ракового поражения. Обследование проводится не только на пораженной, но и на здоровой груди, для того, чтобы выявить наличие метастазов. Обязательным является пальпация надключичных и подмышечных впадин. Если симптоматика злокачественного новообразования четко выражена, то постановка диагноза не составляет труда. Но при заболевании на начальных стадиях, малых размерах или глубоком расположении опухоли, проводится дополнительная диагностика.
В качестве дополнительной диагностики используется бесконтрастная маммография, рентгенография, аспирационная биопсия, пункция с цитологическим исследованием. Возможно частичное иссечение опухоли вместе с окружающими тканями и проведение гистологического исследования. Если наличие рака подтверждается, то операцию расширяют до радикальной. Для определения степени распространения злокачественной опухоли в организме, пациентке проводят сцинтиграфию скелета, ультразвуковое исследование печени, рентгенографию костей и рентген легких.
Ранняя диагностика рака молочной железы
Ранняя диагностика рака молочной железы носит комплексный подход, который состоит из множества методов, используемых как в медицине, так и в онкологии. Основные цели раннего диагностирования:
- Обнаружение рака на ранней стадии (именно в этот период можно провести успешное лечение).
- Выбор врачом эффективного и идеально подходящего метода лечения.
- Оценка результатов терапии.
Диагностика должна дать ответ на такие вопросы, как: какой тип опухоли (инвазивный или неинвазивный), есть ли метастазы в соседних лимфоузлах, если да, то насколько велико поражение.
Ранняя диагностика делится на первичную и уточняющую:
- Первичной диагностирование
Обследование носит название скрининговой. Ее основная задача выявиться первичные изменения в молочной железе. Это самомообследование груди, пальпация молочных желез, осмотр хирургом, маммологом, онкологом и эндокринологом. Первичная диагностика проводится у женщин без явных признаков изменения в груди. Обследования должны носить регулярный характер, так как их цель – раннее выявление злокачественного новообразования.
- Уточняющие обследования
В этом случае используются методы, позволяющие целенаправленно искать изменения в молочных железах. Диагностика дает возможность уточнить природу, распространенность и характер изменений. Обследования проводятся в течение всего лечения, для контроля его эффективности. Основные диагностические методы данной категории: МРТ, УЗИ, КТ, биопсия и другие.
Ранняя диагностика рака молочной железы осуществляется врачом при каждом посещении женской консультации. Стандартное диагностирование представляет собой пальпацию органа для определения наличия припухлостей и болезненных уплотнений. Такое обследование объясняется тем, что злокачественное новообразование груди чаще всего проявляется как небольшая припухлость, которую в 90% случае женщина обнаруживает самостоятельно. Во время обследования, осмотр проводится в освещенном помещении, в вертикальном и горизонтальном положении, с поднятыми и опущенными руками.
В процессе осмотра врач обращает внимание на ряд факторов, которые могут свидетельствовать о наличие патологии: припухлости или уплотнение груди (сосков), покраснение или отечность кожи, асимметрия, изменение очертаний и положения соска. Деформация ареолов, выделения из сосков, втяжение кожи на груди, шелушение груди, опухолевые уплотнения в подмышечной впадине, припухлости плече, боль и дискомфорт в груди, также свидетельствуют о патологическом процессе.
Очень часто явные признаки рака диагностируют на поздних стадиях, когда опухоль приобретает запущенную форму. В этом случае плотное болезненное новообразование прорастает в грудную стенку, что приводит к обездвиживанию груди. Из-за прорастания опухоли на кожный покров, молочная железа изъязвляется, деформируется, втягивается сосок. Из соска могут появляться кровянистые выделения. Если опухоль прорастает в лимфатические узлы, то это приводит к увеличению подмышечных лимфоузлов, из-за чего появляются болезненные ощущения и дискомфорт.
 [4]
[4]
Дифференциальная диагностика рака молочной железы
Дифференциальная диагностика рака молочной железы – это обследования, которые позволяют исключить по тем или иным факторам и симптомам заболевания, что в конечном итоге позволит диагностировать единственно вероятное поражение. Дифференциальное обследование рака груди, в первую очередь проводится с фиброаденомой и мастопатией. К примеру, липома в отличие от злокачественного новообразования мягкая на ощупь, без уплотнений и имеет крупнодольчатое строение. Если есть киста, то она может достигать больших размеров, что существенно затрудняет диагностику. В этом случае, для постановки правильного диагноза проводится пункционная биопсия или резекция груди.
- При дифференциальной диагностики рака и галактоцеле, необходимо обращать внимание на то, что последнее заболевание развивается в период лактации. По своей структуре галактоцеде напоминает кисту и в течение долгого периода времени не меняет размеров.
- В некоторых случаях, наличие добавочной молочной железы, которая располагается у края большой мышцы груди и существенно увеличивается в размерах в период лактации, напоминая шишку, может ошибочно напоминать злокачественное новообразование.
- При ангиоме груди, поражение не имеет четких границ, уменьшается при сдавливании и мягкое на ощупь. Если ангиома находится под кожей, то кожный покров приобретает голубоватый окрас.
Сложности возникают при дифференциальном диагнозе рака молочной железы и мастита. Мастит характеризуется острым началом, сильными болезненными ощущениями, высокой температурой. Но если состояние не улучшает в течение нескольких дней и данная симптоматика появилась вне периода лактации или у женщины пожилого возраста, то это может быть признаком рака груди.
Согласно статистическим данным, большинство женщин самостоятельно обнаруживают опухоль, но не придают ей должного значения. Из-за позднего обращения за медицинской помощью, рак молочной железы принимает необратимый патологический характер, что приводит к летальному исходу.
Методы диагностики рака молочной железы
Методы диагностики рака молочной железы – это комплекс процедур и исследований, позволяющих выявить патологические изменения, определить их природу, характер течения и ряд других показателей. Рассмотрим основные методы исследования, используемые при постановке диагноза:
Маммография
На сегодняшний день маммография является основным и самым эффективным методом раннего диагностирования рака груди. Процедура является скрининговым обследованием и проводится на специальных аппаратах, которые позволяют распознать патологический рост и изменения в тканях. Полученные снимки сравнивают со снимками здоровой груди. В процессе маммографии, грудь сжимается пластинами, для того чтобы сделать снимки с разных ракурсов. Ткани органа на снимке имеют белый цвет, жировая – прозрачный, а уплотнения и патологические участки четко очерчены.
Маммография дает возможность распознать первичные и вторичные признаки злокачественного процесса.
- Первичные признаки – микрокальцинаты и опухолевая тень, которая имеет звездчатую или неправильную форму с неровными контурами. Опухоль может сопровождаться тропинкой к соску и вызывать его втяжение, кожа уплотнена, имеет изъязвления. Если на груди есть микрокальцинаты, то есть отложения солей кальция в стенках протоков желез, то это указывает на большую вероятность злокачественного процесса в груди.
- Вторичные признаки – характеризуются разнообразной симптоматикой, которая проявляется в изменениях кожного покрова, сосков и тканей, окружающих новообразование.
Компьютерная томография
КТ молочных желез позволяет отследить распространение опухолевых очагов и метастаз. Проводится как при ранней диагностике рака молочной железы, так и в процессе всего курса лечения, для контроля результатов терапии.
 [10]
[10]
Магнитно-резонансная томография
МРТ молочных желез проводится с помощью мощного магнитного поля. Молочные железы облучаются электромагнитными волнами. В результате электромагнитная энергия фиксируется специальными датчиками и обрабатывается компьютером.
Позитронно-эмиссионная томография
Является радионуклидным томографическим методом, который быстро и точно определяет наличие опухолевых процессов. В процессе диагностирования, в железы вводится радиофармпрепарат, содержащий радионуклиды с позитронным бета-распадом.
ПЭТ позволяет установить наличие злокачественного новообразования, обнаружить метастазы, определить остались ли раковые клетки после проведенного лечения и отличить рак от доброкачественных заболеваний и воспалительных процессов.
Биопсия при раке молочной железы
Биопсия – это взятие анализа из опухоли с последующим цитологическим исследованием. Преимущества метода в его невысокой стоимости, простоте выполнения и безболезненности. Очень часто биопсию проводят под контролем ультразвукового мониторинга. Биопсия может проводиться путем оперативного вмешательства или с помощью секторальной резекции. Процедура проводится в условиях амбулатории с обезболиванием и не требует специальной подготовки.
Диагностическое исследование позволяет идентифицировать тип новообразования. Биопсия определяет гормонозависимые опухоли с помощью иммуногистохимических тестов. От гормонального статуса опухоли зависит методика лечения и прогноз на выздоровление. С помощью биопсии удается определить гистогенез злокачественного новообразования и разработать эффективный план лечения, определить чувствительность раковых клеток к различным видам терапии.
- Тонкоигольная аспирационная биопсия – самый простой и быстрый метод диагностики. Проводится с помощью тонкой иглы, поэтому не требует анестезии.
- Трепан-биопсия – проводится в условиях амбулатории, но с анестезией. Игла вводится в ткани под контролем УЗИ.
- Хирургическая биопсия – используется в тех случаях, когда теран-биопсия и тонкоигольная не подтвердили наличие онкологии. Процедура проводится при условии полной госпитализации и под общей анестезией. Врачи проводят операционное вмешательство и исследуют удаленную опухоль.
Термография
Диагностический метод, заключающийся в измерении температуры кожного покрова груди. Исследование основано на различии в температурных значениях у опухолевых и здоровых тканей. Поскольку новообразование имеет большое количество кровеносных сосудов, то они излучают тепло, которое можно обнаружить с помощью термографии.
Данный метод диагностики не приобрел широкого применения, так как имеет большое количество ложноотрицательных результатов.
Световое сканирование
Относится к самым современным диагностическим методам. Суть исследования в том, что через ткани молочной железы пропускают инфракрасный цвет, который позволяет определить наличие опухолевых узлов и метастазов.
Единственный недостаток данного метода – повышенная чувствительность и недостаточная специфичность.
Галактофорография
Проводится при наличии выделений кровянистого характера из сосков. В млечные протоки контрастное вещество, которое выявляет множественные и одиночные папилломы и внутрипротоковый рак.
Пневмоцистография
При данном диагностическом исследовании в пораженную полость молочной железы вводят газ. Методика дает возможность выявить внутрикистозные патологические разрастания.
Помимо вышеописанных методов диагностики рака, пациентке проводят рентгенографическое исследование легких, КТ органов брюшной полости и грудной клетки, УЗИ лимфоузлов и органов брюшной полости. Обязательными являются общеклинические анализы и обследования, а также радиоизотопные исследования скелета, то есть сцинтиграфия.
Подобное диагностирование поможет оценить степень распространения злокачественной опухоли в организме, наличие или отсутствие метастазов в лимфатических узлах и других органах. Результаты проведенных исследований позволяют выяснить характеристики и особенности патологии, а также состояние организма. Обратите внимание, для наблюдения за течением заболевания, контроля лечения и выявления рецидивов используется онкомаркер рака молочной железы СА15-3.
Анализы при раке молочной железы
Анализы при раке молочной железы дают возможность узнать особенности патологического заболевания. По результатам исследования врач диагностирует ту или иную форму рака груди и стадию опухолевого процесса. Для проведения анализов у больной берут кровь и ткани из пораженной области.
- Своевременная диагностика и сдача анализов позволяет выявить и предотвратить рецидивы злокачественного новообразования, проверить организм на наличие раковых клеток после проведенной операции или терапии.
- Анализы позволяют обнаружить опухоль на самых ранних стадиях, и определить находится ли человек в группе риска.
При анализе крови, изучению подлежат опухолевые маркеры: CA 15-3, СА 125 II, CYFRA 21-1, СА 72-4 и раковый эмбриональный антиген (РЭА). Если данные показатели выше нормы, то это может указывать как на злокачественное, так и на доброкачественное образование.
Муциноподобный раковый антиген CA 15-3 находится в мембранах раковых клеток. Нормой считаются значения от 0 до 26,9 ед/мл. Анализы крови сдаются в динамике, это позволяет определить скорость роста опухоли, риск метастазирования и рецидивов злокачественного новообразования. Дополнительным подтверждающим анализом является альфа-фетопротеин. Нормальный показатель АФП считается от 0 до 7,51 ед/мл. При отклонениях от нормы можно говорить о патологических процессах в организме.
При исследовании тканей проводится иммуногистохимический анализ на рак молочной железы. Для его проведения используют специальные реактивы, которые содержат антитела со специальными веществами и ткани молочной железы, которые берут с помощью биопсии. Анализ основан на антиген-антитело реакции. Так, при попадании в организм сторонних агентов в крови происходит реакция, которая их блокирует. Иммуногистохимический анализ позволяет выявить искомый антиген раковой опухоли, поэтому его проведение очень важно для составления плана лечения.
Онкомаркеры при раке молочной железы
Онкомаркеры при раке молочной железы представляют собой белки, которые циркулируют в крови. Уровень белков повышается при онкологических заболеваниях. Но повышенная концентрация может наблюдаться и в организме здорового человека. Именно поэтому онкомаркеры используются в качестве вспомогательного диагностического метода, который позволяет выявить рецидивы заболевания и оценить эффективность лечения.
К примеру, онкомаркер СА 15-3 является маркером рака молочной железы и яичников, а СА 125 – это маркер, указывающий на рецидивы опухолевый процессов в груди и яичниках. Для диагностики также используют TRU-QUANT и СА 27-29 маркеры.
Повышенный уровень данного маркера свидетельствует о раковом процессе. Так, при диагностике карциномы, уровень специфичность СА 15-3 составляет 95%, в отличие от доброкачественных новообразований. СА 15-3 прямо пропорционален размеру опухолевого поражения. То есть повышенные значения могут указывать на вовлеченность лимфоузлов в онкопроцесс. Если онкомаркер возрастает на 25%, то это говорит о прогрессировании злокачественного новообразования. Если уровень снижается, то лечение эффективно и рак отступает.
СА 15-3 позволяет узнать о наличии метастазов и рецидивировании заболевания. Если рак молочной железы лечили с помощью химиотерапии или радиотерапии, то значения СА 15-3 могут временно подниматься. Это указывает на то, что опухоль разрушается, то есть терапия действенна. Но зафиксированы случаи, когда СА 15-3 имел повышенные значения у беременных, но это не являлось признаком злокачественного новообразования.
- Онкомаркеры СА 15-3 и РЭА
Данные онкомаркеры позволяют отслеживать развитие опухоли. Очень часто СА 15-3 проводят одновременно с раково-эмбриональные агентом, то есть РЭА, который относится к маркерам онкологии прямой кишки.
Нормальным показателем СА 15-3 считается от 0-27 Ед/мл. Если значения онкомаркера выше указанной нормы, то это указывает на метастазирующий процесс. Норма РЭА от 0-5 Ед/мл. Расшифровка онкомаркеров должна осуществляться только врачом. Рак не диагностируют только по повышенному уровню СА 15-3 или другого онкомаркера. Для подтверждения заболевания проводится комплексная диагностика.
Диагностика рака молочной железы заключается в комплексном подходе к выявлению злокачественного новообразования, определению ее типа и других особенностей течения заболевания. От своевременности проведения диагностирования и ее эффективности зависит выбор методов лечения. Чем раньше будет обнаружен рак, тем лучше прогноз и выше шансы на выздоровление.

